Questões Militares
Foram encontradas 130.246 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
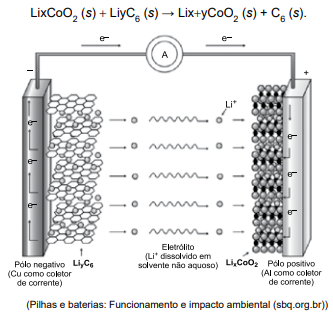
De acordo com o esquema, durante a descarga da bateria
Considere o diagrama de fases para a substância hidrazina, usada em propelentes de foguetes.
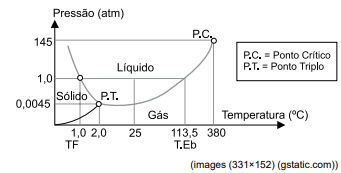
Na temperatura de 390 ºC, a hidrazina é um
I. ETÓXI-METANO II. PENTANOL III. ÁCIDO METANOICO IV. ETANAL V. PENT-2-ONA
Estabelecem ligações intermoleculares do tipo ligação de hidrogênio e possuem a maior solubilidade em água, respectivamente, os compostos:
MnO4 – (aq) + H2 O2 (aq) + H+ (aq) → Mn2+ (aq) + O2 (g) + H2 O(l)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2 O2 ; E0 = + 0,68 V MnO4 – (aq) + 8 H+ (aq) + 5 e– → Mn2+(aq) + 4 H2 O(l); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
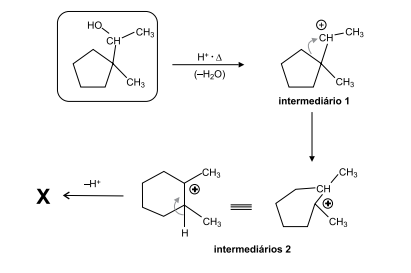 (Solomons. Adaptado)
(Solomons. Adaptado)A estrutura de X que representa o produto principal da reação é:
A pirâmide olfativa usada na formulação de perfumes considera a volatilidade das substâncias.
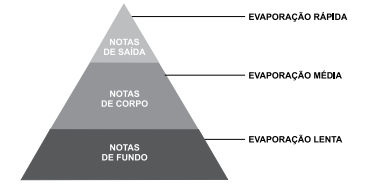
(O que significa no perfume as notas de saída, corpo e fundo? Moda Masculina Journal. Adaptado)
A tabela reúne a pressão de vapor de algumas substâncias a 25 ºC e respectivos aromas.
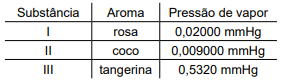
De acordo com as informações fornecidas, pode-se concluir que é nota de saída, de corpo e de fundo, respectivamente,
14 KMnO4 + 4 C3 H5 (OH)3 → 7 K2 CO3 + 7 Mn2 O3 + 5 CO2 + 16 H2 O
O agente oxidante e a variação do número de oxidação do elemento manganês nessa reação são, respectivamente,
2 H2 S(g) + 3 O2 (g) → 2 SO2 (g) + 2 H2 O(g)
A tabela reúne as entalpias de formação dos componentes da reação.

Portanto, a entalpia da reação, em kJ.mol–1 de H2 S(g), é, aproximadamente,
I. Amaciamento de carne pela adição de papaína. II. Conservação de frutas em geladeira. III. Antiácido efervescente em pó colocado na água.
Os fatores que alteram a rapidez das reações nas situações I, II e III são, respectivamente,
Considere a reação a seguir:
2 NO + 2 H2 → N2 + 2 H2 O
A lei da velocidade para a reação é de segunda ordem
para o NO e de primeira ordem para o H2
. Portanto, ao
dobrar a concentração de NO mantendo-se a concentração de H2
, a velocidade da reação é:
Considere a estrutura a seguir:
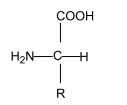
A estrutura química representada é a fórmula geral dos ______________ . A formação de cadeia polimérica dessas estruturas se dá por _________, formando um ___________.
As lacunas são preenchidas, correta e respectivamente,
por:
A reação a seguir representa uma reação de substituição nucleofílica.
2 CH3 OH + (CH3 )3 CCl → (CH3) 3 COCH3 + CH3 OH2 + + Cl-
Nessa reação, o nome do reagente oxigenado e a função
orgânica do produto não iônico são, respectivamente
2 H2 S(g) + SO2 (g)
 3 S(s) + 2 H2
O(g); ΔH < 0
3 S(s) + 2 H2
O(g); ΔH < 0 Ocorre o deslocamento do equilíbrio no sentido dos produtos quando, nesse sistema,