Questões de Concurso Sobre engenharia química e química industrial
Foram encontradas 2.374 questões
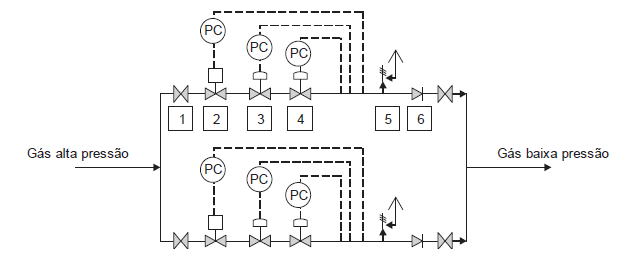 Os equipamentos que compõem esta estação, conforme a sequência numérica, são:
Os equipamentos que compõem esta estação, conforme a sequência numérica, são:A tabela abaixo mostra os resultados da DBO5,20 (Demanda Bioquímica de Oxigênio) e DQO (Demanda Química de Oxigênio) após dois processos de tratamentos realizados para diminuir a carga a poluidora de um efluente líquido.
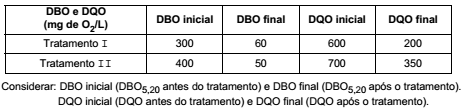
Observando-se os resultados e considerando-se que não há interferentes nas determinações da DBO e da DQO, o tratamento
A figura abaixo mostra uma carta de controle de Shewhart para medidas de pH de uma solução com pH igual a sete. A carta de controle mostra os resultados das médias de várias medições realizadas.
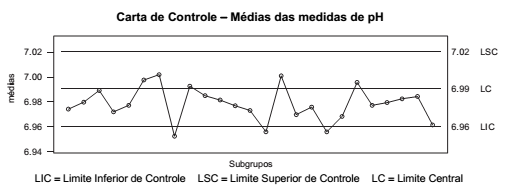
Sobre o gráfico apresentado, considere:
I. O processo de medição para este valor de pH (7,0) nas condições estabelecidas está sob controle estatístico.
II. O gráfico de médias apresenta tendência descendente em relação ao Limite Central.
III. Ações corretivas devem ser feitas para eliminação das causas comuns ou aleatórias que resultaram em pontos fora dos limites de controle.
Está correto o que consta APENAS em
O sistema de filtração denominado ..I.. baseia-se em um processo mecânico que tem como objetivo a desidratação do lodo. É constituído por placas dispostas de forma sequencial onde são colocados os elementos filtrantes. No processo, o lodo é bombeado, forçando a passagem do líquido, sob pressão, pelo meio filtrante, onde os sólidos são retidos.
A lacuna I é preenchida corretamente por
Observe, a seguir, o diagrama de fases quando duas substâncias estão misturadas e aquecidas, como ocorre, por exemplo, num processo de destilação simples.
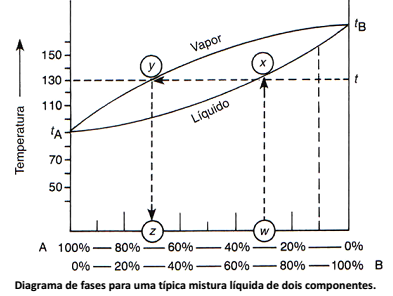
De acordo com o diagrama apresentado, analise as afirmativas.
I. Mostra o comportamento de uma mistura de dois líquidos numa destilação simples; as linhas horizontais representam temperaturas constantes. A curva superior representa a composição do vapor e a curva inferior se refere à composição do líquido.
II. Para qualquer temperatura constante (linha horizontal), como, por exemplo, a linha t, a intersecção da linha com as curvas dão as composições do líquido e do vapor durante a destilação, que estão em equilíbrio entre si, naquela temperatura t.
III. No diagrama observa‐se que à temperatura t, a intersecção da curva em x indica que o líquido da composição w estará em equilíbrio com o vapor da composição z, que corresponde à intersecção em y.
IV. O diagrama mostra que, teoricamente, a destilação simples não poderia ser usada para separar A e B, pois sempre haverá a mistura de A e B em qualquer temperatura, e só haveria 100% de A puro em tA (esquerda do diagrama) e 100% de B puro em tB (direita do diagrama). Entretanto, é possível fazer uma separação aceitável da mistura de A e B, por destilação simples, em seus componentes relativamente puros, se a diferença entre os pontos de ebulição de A e B for maior do que 100°C.
Estão corretas as afirmativas
Analise o seguinte diagrama de fases quando duas substâncias estão misturadas e aquecidas, como ocorre, por exemplo, num processo de destilação fracionada.
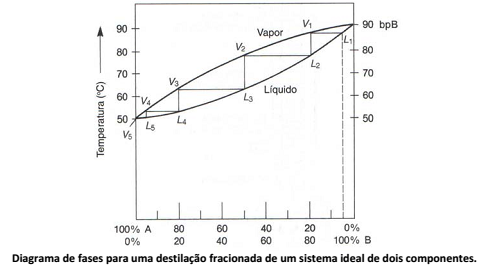
Diante do exposto, assinale a afirmativa INCORRETA.
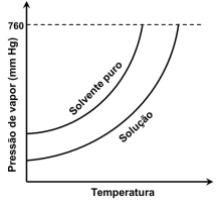
A partir do gráfico, é CORRETO afirmar:
A Figura abaixo mostra um diagrama de fases de uma substância pura.
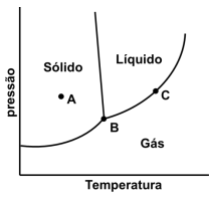
O número de fases que estão presentes em cada um dos pontos circulares identificados como A, B e C,
respectivamente, nessa figura, é
A reação de síntese da amônia em fase gasosa
3H2(g) + N2(g) → 2NH3(g)
é acompanhada por variações de entalpia e de entropia do sistema.
As variações de entalpia (kJ) e entropia (J.K-1) em função da temperatura são apresentadas nas figuras a seguir.
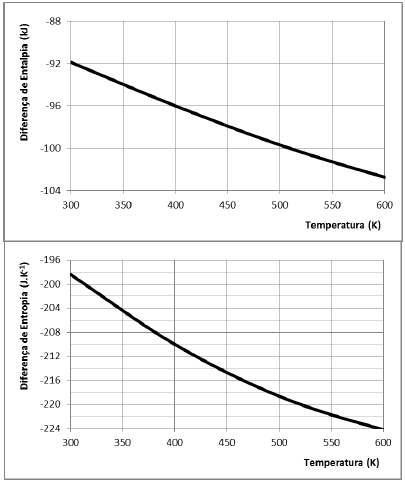
Utilizando os dados apresentados, o valor da energia livre de
Gibbs, em kJ, a 400 K é de
A reação de síntese da amônia em fase gasosa
3H2
(g) + N2
(g)  2NH3
(g)
2NH3
(g)
é acompanhada por variações de entalpia e de entropia do sistema.
As variações de entalpia (kJ) e entropia (J.K–1 ) em função da temperatura são apresentadas nas figuras a seguir.
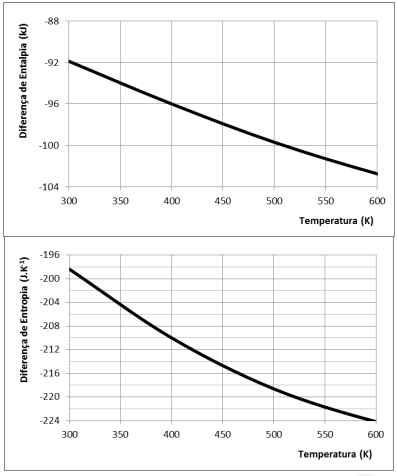
Utilizando os dados apresentados, o valor da energia livre de
Gibbs, em kJ, a 400 K é de
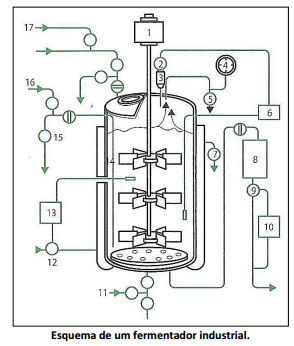
De acordo com o esquema de um fermentador industrial exposto anteriormente, analise as afirmativas. I. O número 3 representado no esquema é filtro de ar. II. O número 7 representado no esquema é saída de água de resfriamento. III. O número 1 representado no esquema é o motor. Está(ão) correta(s) apenas a(s) afirmativa(s)
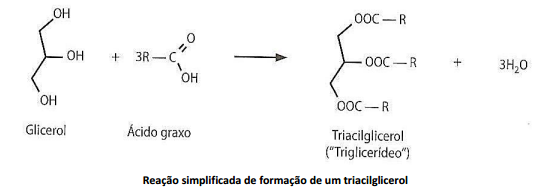
Sobre a obtenção e refino do óleo, é INCORRETO afirmar que