Questões de Concurso
Sobre 1ª lei da termodinâmica em física
Foram encontradas 150 questões
I Fluxo de energia uniforme. II Temperatura uniforme. III Pressão uniforme. IV Composição química uniforme.
Das propriedades, estão corretas:
Assinale a alternativa CORRETA que apresente a relação correta para o trabalho W realizado sobre o sistema formado pelos gases A e B:
Utilize o Texto 03, que traz a descrição de um experimento, para responder à questão.
TEXTO 03
EXPERIMENTO DE CIÊNCIAS PARA O ENSINO FUNDAMENTAL II
Passo 01: A professora acondicionou algumas gotas de detergente em uma seringa descartável sem agulha de 20ml e colocou a parte móvel da seringa (êmbolo). Então, repetiu por diversas vezes os movimentos de puxar e empurrar sem expulsar o líquido, a fim de, apenas, lubrificar a parte interna da seringa. Em seguida, deixou o êmbolo parado na posição equivalente a 10ml e, com massa de modelar, vedou a ponta da seringa para evitar a saída de ar.
Passo 02: A professora encheu um copo com água quente e ao lado deixou um recipiente com gelo.
Passo 03: A professora mergulhou a seringa na água quente e pediu que a turma observasse o que estava acontecendo com o êmbolo da seringa.
Passo 03: A professora retirou cuidadosamente a seringa da água quente e a colocou no recipiente com gelo, demandando, novamente, que a turma observasse o que estava acontecendo com o êmbolo da seringa.
Toda matéria é constituída de partículas, átomos e moléculas, em constante agitação. Quanto mais quente estiver um corpo, maior o movimento, a agitação, a vibração e a energia cinética de cada uma de suas partículas. A temperatura é uma grandeza física que permite avaliar a agitação média dessas partículas.
Fernando Gewandsnadjer. Ciências − matéria e energia, 9. São Paulo: Editora ática, 2016.
Sobre este tipo de transformação, assinale a afirmativa correta.
( ) A entropia é usada para determinar se um processo é espontâneo ou não, enquanto a primeira lei da termodinâmica diz se ele pode acontecer ou não.
( ) A variação de entropia de um sistema isolado que pode evoluir espontaneamente nunca é menor que zero, levando o sistema a evoluir para o equilíbrio onde a entropia é máxima.
( ) A variação de entropia para um processo reversível é calculada como função do calor trocado (Q) e da temperatura do sistema (T).
( ) A entropia explica a espontaneidade do derretimento de uma pedra de gelo, que ocorre para quaisquer condições do meio.
As afirmativas são, respectivamente,
I. A Primeira Lei da Termodinâmica, também conhecida como Lei da Conservação de Energia, afirma que a energia total de um sistema isolado é constante.
II. A Segunda Lei da Termodinâmica estabelece que a entropia de um sistema isolado sempre diminui com o tempo.
III. Em um processo adiabático, não há transferência de calor entre o sistema e seu ambiente.
IV. A eficiência de um ciclo de Carnot é independente das temperaturas das fontes quente e fria.
V. A Terceira Lei da Termodinâmica implica que é impossível atingir o zero absoluto em um número finito de etapas.
Marque a opção que apresenta as afirmativas CORRETAS.
Quando se faz uma vitamina de frutas em um liquidificador, ao ligá-lo, parte da energia elétrica é transformada em energia térmica.
Julgue o enunciado acima, e marque a alternativa CORRETA:
Considere um líquido incolor. Durante a fusão, sob pressão atmosférica constante, a temperatura variou de X °C, no início da mudança de estado, até X + 5 °C, ao final da mudança.
Sobre este líquido, é correto afirmar que ele é uma
Julgue o item a seguir.
A Primeira Lei da Termodinâmica afirma que a energia
sempre permanece constante em um sistema isolado.
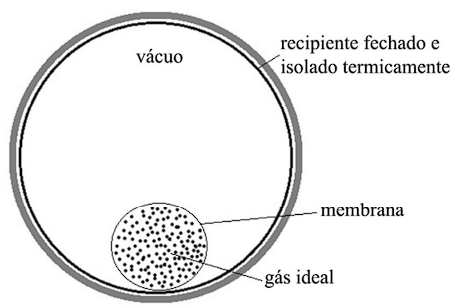
Tendo como referência a figura precedente, que representa um recipiente fechado e isolado termicamente, julgue o item a seguir.
No processo de expansão do gás ideal em razão do
rompimento da membrana, que ocorre dentro de um recipiente
rígido, fechado e isolado termicamente, a temperatura do gás
diminui.
Tendo como referência a figura precedente, que representa um recipiente fechado e isolado termicamente, julgue o item a seguir.
Quando submetido a condições de alta pressão e alta
temperatura, o comportamento de um gás real tende a se
aproximar ao de um gás ideal.
A Primeira Lei da Termodinâmica estabelece que a variação da energia interna (ΔU) de um sistema é dada pela diferença entre o calor trocado com o ambiente (Q) e o trabalho realizado no processo termodinâmico (W), da seguinte forma: ΔU = Q - W. Assim, quando o trabalho realizado pelo sistema for igual ao calor fornecido a ele, haverá uma transformação
Considere o ciclo termodinâmico teórico apresentado no diagrama PV, da Figura 4, no qual um mol de um gás monoatômico ideal está contido em um cilindro com pistão. O ciclo é composto por quatro etapas distintas: uma expansão isobárica (A ➝ B); uma expansão isotérmica (B ➝ C) à temperatura de 562,5 K; uma transformação isocórica (C ➝ D); uma compressão isotérmica (D ➝ A) à temperatura de 300 K. Para efeitos de cálculo, utilize a constante dos gases ideais R = 8 J/(mol · K) e In 1,5 × 105 ≅ 12.
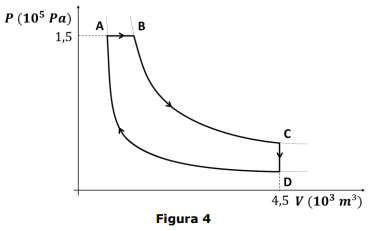
Considerando a situação apresentada na Figura 4, analise as seguintes assertivas:
I. O volume do gás no estado A é de 1,6 × 10−2 m3.
II. A pressão do gás no estado C é de 103 Pa.
III. O trabalho realizado pelo gás no processo B ➙ C é de aproximadamente 54 kJ.
IV. O trabalho realizado pelo gás no processo A ➙ B é de 210 J.
Quais estão corretas?