Questões de Concurso
Sobre calorimetria em física
Foram encontradas 253 questões
Uma usina hipotética geradora de energia elétrica tem como característica a geração de energia pelos processos hidrelétrico e termelétrico, mas não simultaneamente. Por causa da natureza da geração hidrelétrica, a usina foi construída próxima de um rio.
A geração termelétrica só entra em operação em períodos de escassez de água na represa usada para movimentar as turbinas dos geradores ou em períodos de manutenção dos equipamentos da hidrelétrica.
Os geradores termelétricos operam a partir do calor produzido pela queima de carvão mineral. Na sala de geradores termelétricos, há um sistema de ventilação forçada que substitui equipamentos de ar condicionado, por conta de um melhor aproveitamento da energia consumida no local, e cuja função é manter a temperatura ambiente próxima de 23°C.
Um dos ambientes da usina está sendo criado para acomodar uma guilhotina elétrica a ser usada para corte de placas de cobre de um sistema de ionização usado em partes da planta industrial para tratamento da água, antes de retorná-la ao leito do rio.
O diagrama unifilar da iluminação da sala onde ficará a guilhotina está ilustrado na Figura I e a placa de especificações do motor da guilhotina está ilustrada na Figura II.

Dados: Calor específico do gelo = 0,50 cal/g °C Calor específico da água = 1,0 cal/g °C Calor específico do vapor de água = 0,50 cal/g °C Calor latente de fusão do gelo = 80 cal/g Calor latente de vaporização da água = 540 cal/g
Uma substância pura apresenta as seguintes características:
− calor específico no estado líquido = 0,40 cal/g °C;
− temperatura de fusão = 10 °C;
− temperatura de ebulição = 70 °C;
− calor latente de vaporização = 80 cal/g.
Num frasco de capacidade térmica desprezível são colocados 10 g dessa substância à temperatura ambiente de 20 °C. Até que ocorra a vaporização completa dessa amostra da substância, uma fonte térmica deverá fornecer-lhe energia, em joules, de
Dado:
1 cal = 4,2 J
Halliday e Resnick. Fundamentos de Física: gravitação, ondas e termodinâmica. v. 2. Rio de Janeiro: LTC, 2009 (com adaptações).
A partir do texto acima, assinale a alternativa que apresenta a quantidade de calor que uma amostra de gelo de massa m = 100 g a -10 °C deve absorver para passar ao estado líquido a 20 °C, sendo o calor específico do gelo (cgelo) igual a 2.220 J/kg.K, o calor específico da água (cágua) igual a 4.190 J/kg.K e o calor de fusão do gelo (LF) igual a 333 kJ/kg.
• Thayla e Júnior moram em Fortaleza (nível do mar); • O calor latente de fusão do gelo é de 80 cal/g; • O calor específico da água é de 1 cal/g ºC; • 1 cal equivale, aproximadamente, a 4 joules.
Considerando que Thayla vai usar este micro-ondas sempre na potência máxima, o tempo necessário para a água entrar em ebulição é, aproximadamente, de
Os dados coletados durante um experimento estão expressos na tabela abaixo:

Segundo a lei de Charles, a relação entre o volume e a temperatura, à pressão constante, é linear: V = kT. De acordo com os dados da tabela, o valor dessa constante k, em ml/K, é aproximadamente:
A1- Considere que um cilindro de cobre de massa M, à temperatura de 80 ºC, é completamente mergulhado em água, a 20 ºC, contida num recipiente isolante de calor. Considere que a massa de água é igual à massa do cilindro de cobre. Sabendo que o calor específico da água é cerca de 10 vezes maior que o do cobre, a temperatura de equilíbrio da água será de 50 ºC. A2- A quantidade de calor necessária para elevar a temperatura de um gás ideal em 1 ºC é menor sob pressão constante do que sob volume constante. A3- A pressão de um gás ideal em um container de volume constante é proporcional à energia cinética média das moléculas do gás.
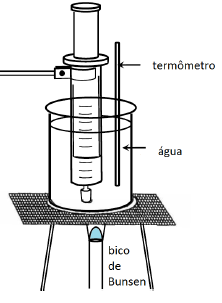
Para determinar o equivalente mecânico do calor (J), um grupo de alunos usou um tubo isolante, com comprimento interno de 1,00 m, um termômetro e várias bolinhas de ferro, de tamanho desprezível e calor específico 0,10 cal/(g.°C). O tubo é dotado de uma tampa com furo por onde pode ser inserido o termômetro, que fica com seu bulbo inserido dentro do tubo. As bolinhas são depositadas no fundo do tubo (figura 1). É medida a temperatura inicial do sistema: θi = 20,00°C; adota-se o valor da aceleração da gravidade: g = 10 m/s2 . Fechado o tubo, o conjunto é virado de 180° (figura 2) por 50 vezes.
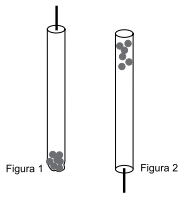
Ao final do procedimento, a temperatura das bolinhas é medida: θf = 21,25 °C.
O equivalente mecânico do calor, assim determinado,
vale, em J/cal,
Energia interna de um sistema (U) é a soma das energias cinética e potencial das partículas que constituem um gás. Esta energia é uma característica do estado termodinâmico e deve ser considerada como mais uma variável que pode ser expressa em termos de pressão, volume, temperatura e número de mols.
Equação da energia interna
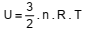
Onde:
U: energia interna do gás
n: número de mol do gás
R: constante universal dos gases perfeitos
T: temperatura absoluta (kelvin)
A energia interna em kJ de 2 mols de um gás perfeito na temperatura de 27°C é, em kJ,
Dado:
R = 8,31 J/mol . K
O calor específico do material que constitui o corpo, em J kg-1 K-1 , corresponde a

A figura precedente representa dois blocos A e B com
massas iguais a 6 kg e 4 kg, respectivamente, inicialmente em
repouso e ligados por um fio ideal (sobre uma roldana igualmente
ideal). O coeficiente de atrito entre A e o plano horizontal vale 0,4
e a aceleração da gravidade vale 10 m/s2
.
Com base nas informações apresentadas e assumindo que toda a energia dissipada pela força de atrito foi usada para aquecer o corpo A, julgue o item a seguir.
Se o corpo A é feito de material que apresenta calor específico
igual a 378 J/kgºC (Cobre), então, após ele ter sido arrastado
por 1cm, sua temperatura terá aumentado em mais de
0,1 milésimos de Kelvins.
Um processo reversível para um sistema pode ser entendido como aquele que permite ser invertido totalmente, sem deixar vestígios em si ou no meio. Considere as afirmativas a seguir:
I - Quando existir expansão livre, o sistema será reversível.
II - A troca de calor com diferença finita de temperatura é um fator de irreversibilidade.
III - Sistemas onde ocorra histerese são irreversíveis.
São corretas as afirmativas:
A figura, a seguir, mostra uma panela usada para preparar o café da manhã.

Durante a preparação, meio litro de água à temperatura
inicial de 20°C (293 K) é fervido à 100°C (373 K). Considerando
o calor específico e a densidade da água iguais a
1 cal/g°C e 1 g/mL, respectivamente, a variação de entropia
desse processo termodinâmico é, em cal/°C, de