Questões de Técnicas em Laboratório para Concurso
Foram encontradas 6.031 questões
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.
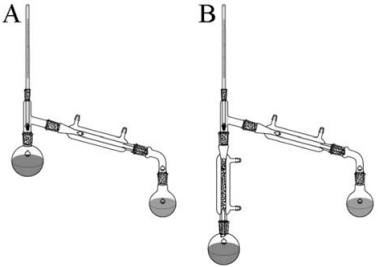
Considerando a figura e as informações precedentes, julgue o item subsequente.
A figura B representa uma montagem usada na filtração a
vácuo.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
As montagens mostradas em A e B na figura são indicadas,
respectivamente, para separação de misturas homogêneas
sólido-líquido e líquido-líquido.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
A força eluente aumenta quando se usam solventes menos
polares na cromatografia líquida de fase reversa.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
A maior limitação da aplicação da cromatografia gasosa é o
fato de que o analito e a amostra devem ser gasosos para
serem introduzidos no equipamento.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
Na filtração, é indicado misturar bem o líquido que contém o
sólido a ser filtrado antes de vertê-lo no funil, para acelerar o
processo de separação.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
Na filtração a vácuo, uma bomba de vácuo suga o líquido a
ser filtrado; o sólido contido nesse líquido é então retido em
um filtro no interior dessa bomba e recuperado ao final da
filtração.
Os métodos e os princípios de separação são técnicas muito utilizadas nos laboratórios e abrangem desde processos mais simples, como filtração e destilação, até métodos analíticos complexos, como as cromatografias líquida e gasosa. A figura a seguir representa dois aparatos comumente utilizados em métodos de separação.

Considerando a figura e as informações precedentes, julgue o item subsequente.
Nas filtrações que utilizam funil cônico de vidro, o papel
filtro deve ser dobrado para ajustar-se perfeitamente ao cone
interno do funil, ao ser molhado com uma pequena
quantidade de água.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
A vidraria mais indicada para medir 8,3 mL de uma solução,
durante uma diluição, é uma pipeta volumétrica de 10 mL.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
O sistema de refrigeração do tipo ultrafreezer é um
equipamento que permite o armazenamento de amostras em
temperaturas de até –273,15 ºC.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
A mufla é um tipo de forno muito utilizado na calcinação de
substâncias e opera em temperaturas maiores que as
alcançadas pelas estufas, tipicamente de 200 ºC a 1.400 ºC.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
Materiais voláteis e corrosivos devem ser manipulados em
capelas de exaustão de gases, e tais capelas devem ser
separadas de acordo com os tipos e as compatibilidades de
materiais nelas manipulados.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
O liofilizador permite a remoção da água e, portanto, a
secagem de materiais por sublimação, sem a necessidade de
aquecimento.
Acerca do uso e da conservação de aparelhagens comuns de laboratório, julgue o item a seguir.
Para a melhor conservação de eletrodos de vidro para a
medida de pH, é indicado o uso de soluções de ácido
fluorídrico 3 mol/L como líquido de repouso para os
eletrodos.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
A partir da diluição de 200 mL de uma solução de sacarose a
150 mg/L, o maior volume possível de se obter de uma
solução diluída a 30 mg/L de sacarose é de 1,0 L.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Considere que o rótulo de um frasco de ácido
clorídrico comercial contenha as seguintes informações:
HCl 37% (massa/massa); densidade = 1,2 g/cm3
; massa
molar = 36,5g/mol. Nesse caso, a partir dessas informações,
é correto afirmar que, se 100 g desse reagente forem
misturados a 163 g de água, então a concentração de HCl da
solução formada será maior que 15% em fração em massa.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Soluções concentradas alcalinas, como as de NaOH, devem
ser estocadas em frascos de vidro, de preferência com
tampas do tipo rolha de vidro esmerilhada.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Uma solução 0,1 mol/L de NaOH tem concentração em
massa maior que 5,0 g/L de NaOH, considerando-se a massa
molar do NaOH igual a 40 g/mol.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Sabendo-se que a concentração do álcool 70%, muito usado
na desinfecção de mãos e superfícies, é expressa em
percentual de fração de massa e considerando-se que a
densidade do etanol puro seja igual a 0,79 g/cm3
e a da água
seja igual a 1,0 g/cm3
, é correto afirmar que 500 mL de uma
solução de etanol a 70% contêm 350 mL de etanol puro.
É atividade essencial do técnico de laboratório o preparo de soluções. Além das propriedades físicas, como densidade, o técnico deve conhecer, na prática, as definições de concentração e saber fazer diluições. É comum preparar, diluir e manipular soluções com concentração expressa em massa, em quantidade de matéria, fração molar e fração em massa. Acerca desse assunto e de aspectos correlatos, julgue o item que se segue.
Após a mistura de 50 mL de uma solução de NaCl
0,10 mol/L e 200 mL de uma solução de CaCl2 0,05 mol/L,
completando-se o volume dessa mistura a 500 mL em um
balão volumétrico, a concentração do íon Cl– em solução
será maior que 4,0×10–2
mol/L.
O hidróxido de sódio, sólido bastante higroscópico e reativo com o CO2 do ar, é comumente utilizado na padronização e na dosagem de soluções ácidas em laboratórios. Normalmente, para essas titulações, são utilizadas soluções diluídas de NaOH. Em relação a esse assunto, julgue o item a seguir.
Quanto maior a massa molar de um reagente, maior será o
erro relativo associado com a pesagem desse reagente,
principalmente no preparo de soluções mais diluídas.