Questões de Concurso
Sobre equipamentos e técnicas básicas em química
Foram encontradas 1.363 questões
Texto 13A6-I

Texto 13A6-I

Texto 13A6-I

O chumbo (Pb) é um metal potencialmente tóxico encontrado em diversas matrizes ambientais. Para determinação de Pb em água, pode-se empregar a técnica de espectrometria de absorção atômica. Considerando a técnica apresentada, julgue os itens a seguir.
I A relação entre a quantidade de luz absorvida e a concentração do analito em padrões conhecidos pode ser usada para determinar concentrações desconhecidas.
II A instrumentação básica requer fonte de luz primária, sistema de atomização, monocromador e detector.
III O sistema queimador-nebulizador é um limitante e possui algumas desvantagens na técnica de absorção atômica em chama.
Assinale a opção correta.
A cromatografia gasosa acoplada a um espectrômetro de massas (CG/EM) pode ser usada para quantificar óleos essenciais. Considere que determinado químico tenha recebido amostra contendo cinamaldeído e eugenol dissolvidos em CH2Cl2. A análise cromatográfica dessa amostra apresentou o cromatograma de ionização total — TIC (total ionisation chromatogram) — mostrado na figura 13A4-I a seguir. A integração do cromatograma revelou que o tempo de retenção do cinamaldeído foi de 8,9 min e a área sob o pico foi de 6.775.518 unidades arbitrárias; ao passo que o eugenol apresentou tempo de retenção de 10,0 min e área sob o pico de 4.143.349 unidades arbitrárias. Para determinar as concentrações dos óleos essenciais presentes na amostra, o químico preparou curvas-padrão de calibração, conforme ilustrado na figura 13A4-II a seguir, em que a abscissa apresenta concentrações dos óleos em µL/mL.
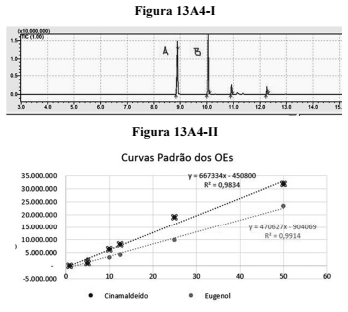
Considerando as informações apresentadas, é correto afirmar que
a concentração de ambos os óleos essenciais na amostra é
( ) A absortividade molar independe do comprimento de onda escolhido.
( ) A concentração de um soluto pode afetar o valor da absortividade molar.
( ) Ao incidir em uma amostra radiação na faixa do infravermelho, os elétrons são excitados a um nível energético superior.
( ) A ressonância magnética nuclear é utilizada para estudar uma grande variedade de núcleos que possuem determinados estados de spin, como, por exemplo, 1H, 13C, 15N, 19F e 31P.
A sequência correta de preenchimento dos parênteses, de cima para baixo, é
Disponível em: https://medidorph.com.br/como-calibrar-um-phmetro-digital/. Acesso em: 21 abr. 2021.
A resposta a essa pergunta é de conhecimento de vários técnicos de química, uma vez que o pHmetro é um dos instrumentos digitais mais utilizados nos laboratórios.
Assinale a alternativa que apresenta o protocolo de calibração do pHmetro que melhor expressa esse procedimento.
Os métodos potenciométricos de análise baseiam-se na medida da diferença de potencial entre dois eletrodos imersos em solução, sem consumo apreciável de corrente. Eletrodos e solução constituem a célula eletroquímica.
Disponível em: https://analiticaqmc.paginas.ufsc.br/files/2013/03/qmc-5318-apostila-20131.pdf. Acesso em: 20 abr. 2021.
Por esse método, é possível determinar a quantidade de ácido fosfórico em refrigerante, desde que sequências concatenadas do procedimento analítico sejam seguidas.
Assinale a alternativa que descreve a sequência correta do procedimento.
Disponível em: http://engesolutions.com.br/wp-content/uploads/2017/04/processo-gravimetria.jpg. Acesso em 15 jun. 2021.
A análise gravimétrica é uma técnica utilizada em laboratórios de química para se medir a massa de determinado composto ou espécie química em uma amostra. A figura acima indica uma série de procedimentos para se chegar à massa do precipitado a partir de uma reação química inicial com uma amostra conhecida.
O precipitado, na gravimetria, deve atender à seguinte característica:
Disponível em: https://www.fq.pt/images/laboratorio/material-para-titulacao.png. Acesso em: 15 jun. 2021.
Os materiais indicados por números são utilizados nos procedimentos de volumetria ácido-base.
Considerando-se essas informações, assinale a alternativa que apresenta os materiais de laboratório descritos corretamente.
A titulação é uma das técnicas mais utilizadas para a determinação da concentração de soluções e de quantidade de matéria em amostras químicas.
A descrição correta do tipo de titulação, utilizada no laboratório, está descrita como
O preparo de soluções é um trabalho recorrente nos laboratórios de química. O procedimento abaixo foi descrito por um auxiliar em química e apresenta alguns procedimentos inadequados.
1º) Medição da massa do sólido com o auxílio de um vidro de relógio com uso cuidadoso da balança digital.
2º) Transferência do sólido para um béquer e, com o uso de uma pisseta, o vidro de relógio foi lavado com o solvente de modo que o líquido de lavagem foi para o béquer.
3º) Adição de solvente ao béquer até a total dissolução do sólido.
4º) Transferência da solução para um balão volumétrico com cuidado ao lavar o béquer.
5º) Homogeneização do conjunto presente no balão volumétrico redondo sem nova adição de solvente.
Um dos procedimentos inadequados realizados pelo auxiliar em química foi