Questões de Concurso Sobre química
Foram encontradas 13.471 questões
São considerados procedimentos corretos para uso e limpeza do microscópio óptico, EXCETO:
O peróxido de hidrogênio, H2O2, quando em contato com um ferimento na pele, é decomposto pela enzima catalase, liberando água e gás oxigênio, conforme reação a seguir.
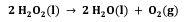
Considerando que 1,3 L de H2O2 (densidade = 1,00 g/mL) se decompõe a 40 °C e pressão de 1,0 atm, assinale a alternativa que apresenta o volume aproximado de gás oxigênio produzido.
Dados:
MM (H2O2) = 34 g/mol.
C = K (Kelvin) – 273
R = 0,082 L.atm/mol.K
Identifique as técnicas clássicas descritas abaixo, respectivamente:
I. Identificação de íons metálicos por meio da cor da chama.
II. Quantificação da concentração de uma substância por meio da adição controlada e quantificada de outra substância reativa de concentração conhecida.
III. Separação e identificação de substâncias pela diferença da temperatura de ebulição dos constituintes.
IV. O analito é convertido numa substância pouco solúvel. O precipitado é filtrado e lavado para remoção de impurezas e convertido, quando necessário, geralmente por meio de um tratamento térmico adequado, em um produto de composição química conhecida. O produto é então pesado.
Alguns procedimentos de laboratório podem parecer simples, porém para que sejam feitos de maneira correta e segura faz-se necessário ter atenção a uma série de detalhes.
Um professor orienta para que os estudantes façam
100 mL de uma solução de NaOH 0,01 mol/L.
Faça os cálculos previamente, tendo atenção na pureza do reagente.
Pese rapidamente a quantidade calculada de
hidróxido de sódio em lentilhas em um béquer,
evitando que o frasco do reagente fique aberto por
muito tempo.
Adicione em torno de 50mL de água destilada no béquer com NaOH, dissolva bem e espere esfriar. Transfira para o balão volumétrico de 100mL utilizando funil, adicione pequenas alíquotas de água destilada no béquer transferindo-as para balão através do funil de forma que o volume não seja completo.
Adicione água destilada até que o menisco fique
próximo da marca de aferição. Faça a aferição do
menisco gotejando com pipeta de Pasteur. Tampe o
balão, faça a homogeneização.
Sobre as instruções do professor, é correto afirmar, exceto:
O trabalho em um laboratório envolve necessariamente um grau de risco; acidentes podem acontecer e acontecem. A adoção rigorosa das normas contribui na prevenção (ou minimização dos efeitos) de acidentes.
Analise as possíveis situações que podem ocorrer e analise as ações tomadas.
I. Uma estudante derramou uma quantidade considerável de ácido acético glacial em sua blusa. No socorro, ela deve ter sua intimidade preservada, portanto deve-se encaminhar a estudante para um banheiro feminino mais próximo para enxágue com água corrente e posteriormente à sala do médico ou enfermeiro da unidade.
II. Para qualquer tipo de acidente, faz-se
necessário procurar o responsável técnico ou
comissão de saúde e segurança do trabalho da
instituição para que as ações de socorro
possam ser executadas conforme o padrão da
instituição.
III. Usuários do laboratório de química que utilizam lentes de contato só podem executar ou acompanhar experimentos se fizerem o uso de óculos de proteção.
IV. No laboratório não se deve levar comida ou bebida. Não tomar líquidos em recipientes de vidro de laboratório. Não fumar no laboratório.
Das situações apresentadas acima, estão corretas:
Identifique os tipos de reações a seguir:
I. CH3-CH2-(CH3)2C-Cl + OH- → CH3-CH2-(CH3)2→C-OH + Cl-
II. CH3-CH2-(CH3)2C-OH + H2SO4 → CH3-CH=C(CH3)2 + H2O + H2SO4
III. III. CH3-CH2-CH2-Cl + OH- → CH3-CH2-CH2- OH + Cl-
IV. CH3-CH2-CH=CH2 + HBr → CH3-CH2-CH(Br)- CH3
V. HOOC-(CH2)4-COOH + H2N-(CH2)6-NH2 → nH2O + [-NH-(CH2)6-NH-CO-(CH2)4-CO-]n
As reações expostas são, respectivamente:
Sobre as limitações de modelos explicativos, identifique os modelos atômicos nas afirmações abaixo:
I. Não explica as conclusões do experimento de Geiger–Marsden que consiste em um feixe de partículas alfa, normalmente executado em uma folha de ouro muito fina em uma câmara evacuada.
II. Não explica a natureza elétrica da Matéria.
III. Não explica o espectro de raia, formado por elementos multieletrônicos.
IV. Não está em acordo com a teoria do eletromagnetismo, que aponta que toda partícula com carga elétrica submetida a uma aceleração origina a emissão de uma onda eletromagnética.
As limitações apresentadas acima são, respectivamente, dos modelos atômicos:
I. Uma amostra de um sólido orgânico de alta pureza a ser analisado para identificar as possíveis funções orgânicas presentes em sua molécula.
II. Uma amostra de um composto orgânico analisada para contribuir na elucidação da estrutura da molécula a partir dos seus fragmentos que geram respostas de razão massa-carga.
III. Determinação da concentração de uma espécie conhecida, a partir da simples relação linear entre absorção da radiação eletromagnética e concentração.
IV. Injeção de uma amostra em uma chama, provocando a excitação eletrônica dos átomos, gerando um sinal analítico através da radiação UV-Vis gerada.
As situações descritas acima estão relacionadas, respectivamente, com as técnicas de:
Um estudante misturou 200mL de solução de ácido HX de concentração 0,1mol/L com 300mL de solução do sal de sódio desse ácido (NaX) que tinha concentração de 0,2mol/L. Sabendo que a constante de ionização do ácido HX é 0,000003. Qual o valor do pH da solução formada?
etanol hidratado 96% (porcentagem em volume) água desnaturante (quantidade desprezível).
Em uma das bateladas de 1000 litros de produto, o analista de controle de qualidade identificou que a concentração alcoólica estava em 70% em volume. O que o operador deve fazer, desconsiderando as possíveis contrações ou dilatações de volume, para que a indústria entregue um produto com concentração próxima e não inferior a 70% INPM (equivalente à 74,5% em volume)?
Dados de densidade: água= 1,0g/mL; etanol= 0,8g/mL.
Quimicamente, a cloroquina (CQ) e a hidroxicloroquina (HCQ) pertencem à classe das 4- aminoquinodinas. Elas têm estrutura central aromática comum, com um cloro na posição 7, ligada às respectivas cadeias laterais básicas. A forma molecular da cloroquina é: C18H26CIN3, com massa molar de 319,9 g/mol. Já a hidroxicloroquina tem massa molar de 335,9 g/mol.
A CQ e a HCQ são administradas como difosfato e sulfato, respectivamente, em suas formas racêmicas.
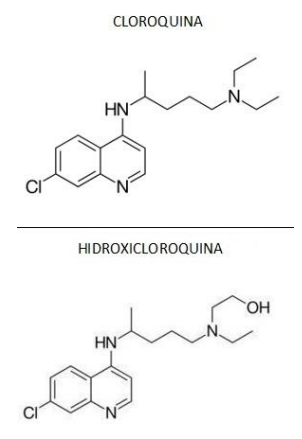
Sobre o medicamento citado acima, marque o que
for correto.
I. A equação
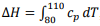 , pode ser usada para
calcular a variação da entalpia associado ao
aquecimento de um mol da substância. II. Se a substância for um líquido ou sólido, o
processo de aquecimento terá praticamente o
mesmo gasto energético a volume constante e
a pressão constante.
III. Se a substância for um gás ideal, o processo de
aquecimento a pressão constante gastará mais
energia que o processo de aquecimento a
volume constante.
, pode ser usada para
calcular a variação da entalpia associado ao
aquecimento de um mol da substância. II. Se a substância for um líquido ou sólido, o
processo de aquecimento terá praticamente o
mesmo gasto energético a volume constante e
a pressão constante.
III. Se a substância for um gás ideal, o processo de
aquecimento a pressão constante gastará mais
energia que o processo de aquecimento a
volume constante. Assinale a alternativa que contém a análise correta.
O dióxido de nitrogênio (NO₂ ) é uma molécula intermediária na produção industrial de ácido nítrico (HNO₃ ), que é muito aplicado na produção de fertilizantes. O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N₂O₄ ), segundo a reação:
2NO₂(g) ⇄ N₂O₄(g) ∆H = −57,23 kJ/mol
Para aumentar o rendimento do dióxido de
nitrogênio na reação, segundo o princípio de Le
Châtelier, deve-se:
(Disponível em: https://jovempan.com.br/noticias/brasil/gas-de-cozinha-atinge-maior-preco-em-2021-e-deve-ficar-ainda- mais-caro-entenda-o-reajuste-da-petrobras.html. Acessado em 28/09/2021)
Supondo que todo o GLP presente no botijão seja somente butano e está totalmente na forma líquida, e que o preço do botijão de gás seja de R$ 125,00, para uma família que teve um gasto mensal com a fatura de gás de R$ 55,77, qual a quantidade de energia que foi liberada, em quilojoules, na queima do gás butano?
A reação de combustão completa do butano (não balanceada):
C₄H₁₀(g) → CO₂ (g) + H₂O ∆H°C = 2.808 kJ/mol