Questões de Concurso Sobre química
Foram encontradas 13.542 questões
Na determinação de Fe (II) e Cu (I) em uma amostra aquosa, empregou-se o reagente complexante 1,10-fenantrolina, em pH ajustado para 4,5. Os complexos formados apresentaram absorção máxima em 511 nm para o Fe (II) e 371 nm para o Cu (I). Observou-se que a determinação de ferro em 511 nm é isenta da interferência de cobre. Entretanto, em 371 nm ambos os complexos metálicos apresentam absorção. Para a amostra analisada a absorvância medida a 371 nm foi 0,800 e a 511 nm a absorvância foi 0,300. A concentração de Fe (II) e Cu (I) em mg/L, na amostra é, respectivamente:
Dados:
Caminho óptico = 1 cm
Absortividades (L. mg−1 . cm−1)
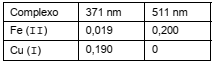
Na combustão da gasolina comum, um de seus componentes − o isooctano é padrão para a qualidade da gasolina. Quanto maior é o índice de octanagem, maior é a compressão que a mistura gasolina-ar suporta no motor, sem detonação prematura; portanto, melhor é a qualidade da gasolina.
A fórmula molecular do isooctano é C8H18. A gasolina pode sofrer combustão completa produzindo CO2 e água ou incompleta − produzindo CO e água ou C (fuligem) e água. Isso ocorre de acordo com a quantidade de oxigênio: combustões completas ocorrem com quantidade de oxigênio suficiente para consumir todo combustível. Por outro lado, a combustão se dá de forma incompleta quando não houver oxigênio suficiente para consumir todo o combustível.
O termo isooctano é um nome indevidamente dado ao composto orgânico cuja fórmula estrutural é representada abaixo.
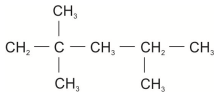
O nome correto (IUPAC) é:
Na combustão da gasolina comum, um de seus componentes − o isooctano é padrão para a qualidade da gasolina. Quanto maior é o índice de octanagem, maior é a compressão que a mistura gasolina-ar suporta no motor, sem detonação prematura; portanto, melhor é a qualidade da gasolina.
A fórmula molecular do isooctano é C8H18. A gasolina pode sofrer combustão completa produzindo CO2 e água ou incompleta − produzindo CO e água ou C (fuligem) e água. Isso ocorre de acordo com a quantidade de oxigênio: combustões completas ocorrem com quantidade de oxigênio suficiente para consumir todo combustível. Por outro lado, a combustão se dá de forma incompleta quando não houver oxigênio suficiente para consumir todo o combustível.
Considere a reação abaixo.

A hidrólise da PCL gera um composto cujo nome é:
A caprolactona pode ser transformada em um polímero sintético biorreabsorvível (policaprolactona ou PCL) muito utilizado em reparação de tecidos humanos.
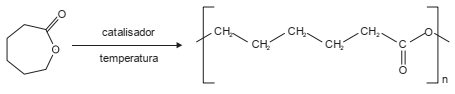
A policaprolactona é um
Deseja-se dessalinizar 1 m3 de água do mar a 25 °C. A pressão osmótica (em atm) a ser aplicada no sistema dessalinizador, considerando-se apenas os íons Na+ e Cℓ − presentes nessa água, é
Dados:
Constante universal dos gases: 0,082 atm . L . mol−1 . K−1
Concentração do sal na água do mar a 25 °C = 2,95 g.L−1
Massas molares (g . mol−1): Na = 23; Cℓ = 35,5
Considerar o NaCℓ totalmente ionizado para cálculo da constante de Van’t Hoff.
Noradrenalina e serotonina são dois neurotransmissores existentes no corpo humano.
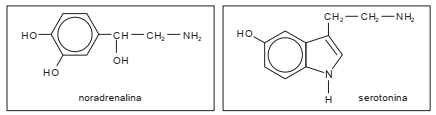
Apresentam em comum as funções:
O quadro abaixo representa os equilíbrios ácido-base entre o ácido sulfuroso e amônia em solução aquosa.
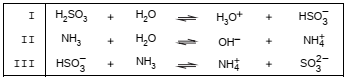
De acordo com a teoria de Brönsted-Lowry,
Considere o quadro abaixo.
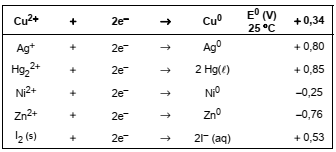
Deseja-se proteger contra a corrosão, chapas de cobre. Analisando-se apenas o potencial padrão de redução deve-se utilizar
A decomposição térmica do calcário produz cal e gás carbônico como mostra a reação e a tabela abaixo.

Está correto afirmar que a
Considere a reação 5 Fe2+ + MnO4− + 8H+ → 5 Fe3+ + Mn2+ + 4 H2O utilizada em uma titulação redox para determinação do teor de ferro em 2 g de uma amostra de minério contendo ferro. Nessa titulação foram gastos 47,5 mL de solução 0,02 mol . L−1 de KMnO4 para alcançar o ponto de equivalência. A porcentagem em massa de ferro na amostra é
Dados:
Massas molares (g . mol−1)
K = 39;
Fe = 56;
Mn = 55; O = 16;
H = 1
Dada a reação não balanceada a seguir:
r Fe2+ + s Cr2O72− + t H+ → u Fe3+ + v Cr3+ + w H2O
Completa r, s, t, u, v e w, correta e respectivamente, os coeficientes
As baterias primárias de lítio são alternativas de fornecimento de energia elétrica de longa duração podendo durar até oito anos. Por isso são utilizados em marca-passo cardíaco. A reação global que ocorre nesse tipo de bateria está representada a seguir.
Dados os potenciais de redução:
Li+ (aq) + e− → Li(s); E° = −3,05 V
I2 (s) + 2e− → 2 I− (aq); E° = + 0,54 V
2 Li(s) + 1 I2(s) → 2 LiI(s)
Com relação a esta pilha afirma-se:
I. O potencial da pilha é de 3,59 V.
II. O cátodo é o lítio metálico.
III. No ânodo ocorre a oxidação do iodo.
IV. O oxidante é o iodo I2.
Está correto o que se afirma APENAS em
Pilhas alcalinas geram corrente elétrica por um período de tempo até 50% mais longo do que uma pilha seca do mesmo tamanho. Considere a reação abaixo, que ocorre nas pilhas alcalinas, e indique a alternativa que apresenta corretamente a reação que ocorre no catodo e no anodo.
Zn(s) + 2 MnO2
(s) → ZnO(s) + Mn2
O3
(s)