Questões de Concurso Sobre química
Foram encontradas 14.919 questões
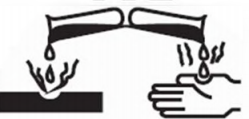
O símbolo de perigo apresentado na figura representa
I. A forma de corrosão denominada uniforme se processa em toda a extensão da superfície, ocorrendo perda uniforme da espessura. II. Todos os metais estão sujeitos ao ataque corrosivo se o meio for sufcientemente agressivo. III. Os metais ouro e prata não sofrem nenhum tipo de corrosão. Está correto o que se afirma em:
A reação química 2H2(g) + 2NO(g) 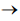 N2(g) + 2H2O(g) ocorre em duas etapas:
N2(g) + 2H2O(g) ocorre em duas etapas:
etapa 1: H2(g) + NO(g) + NO(g) 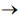 N2O(g) + H2O(g)
N2O(g) + H2O(g)
etapa 2: H2(g) + N2O(g) 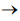 N2(g) + H2O(g)
N2(g) + H2O(g)
Sobre essas reações químicas, é CORRETO afirmar que na etapa
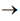 (NH4)3H4P(Mo2O7)6 + H2O
A soma dos coeficientes estequiométricos dessa equação química, após o correto balanceamento, é igual a
(NH4)3H4P(Mo2O7)6 + H2O
A soma dos coeficientes estequiométricos dessa equação química, após o correto balanceamento, é igual a