Questões de Concurso Sobre química
Foram encontradas 13.580 questões
O bombardeamento do urânio-235 com nêutrons induz a um a série de reações de fissão nuclear altamente energéticas. Em uma dessas reações, após a captura de um nêutron (1n), o urânio se desintegra para formar um átomo de césio-137, um isótopo X, e dois outros nêutrons capazes de gerar uma reação em cadeia:
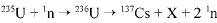
O césio-137 assim formado é um isótopo radioativo que emite radiações gama e beta e pode ser em pregado em radioterapia com o intuito de destruir células cancerosas.
A partir do texto acima e considerando que o tempo de m eia-vida do césio-137 é de 30 anos, julgue o item que se segue.
A radiação beta possui maior poder de penetração que a
radiação gama.
O bombardeamento do urânio-235 com nêutrons induz a um a série de reações de fissão nuclear altamente energéticas. Em uma dessas reações, após a captura de um nêutron (1n), o urânio se desintegra para formar um átomo de césio-137, um isótopo X, e dois outros nêutrons capazes de gerar uma reação em cadeia:
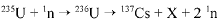
O césio-137 assim formado é um isótopo radioativo que emite radiações gama e beta e pode ser em pregado em radioterapia com o intuito de destruir células cancerosas.
A partir do texto acima e considerando que o tempo de m eia-vida do césio-137 é de 30 anos, julgue o item que se segue.
O isótopo X da reação apresentada consiste em um átomo de 98Sr.
Considerando que foram misturados 6g de KOH com 10g de H2SO4, o valor encontrado para a massa formada de K2SO4 é de, aproximadamente,
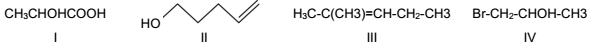
Assinale a opção que indica, corretamente, a isomeria desses compostos.
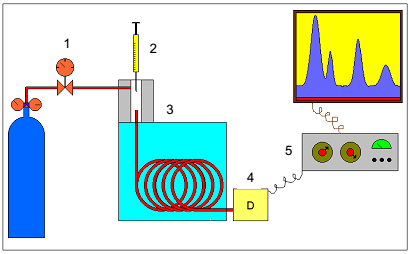
Fonte: adaptada
de<www.biomediconabrasil.com/2012/10metodoscromatograficos.html|?m=1> .
Acesso em: 27 jul. 2015.
As partes do equipamento que estão enumeradas na figura, em ordem crescente, correspondem, respectivamente, a:
Baseando-se nessas informações, é correto afirmar:
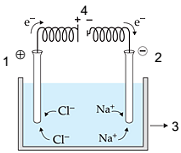
Fonte: adaptado de <www.ohomempodetantoquantosabe.blogspot.com.br>.
Acesso em 20 jul. 2015.
Os componentes 1, 2, 3 e 4 desse sistema são, respectivamente:
Considerando que o teor máximo de acidez do vinagre é de 6,00% de ácido acético, os valores obtidos na análise são
A relação entre a concentração normal (N) e concentração molar (M) para esse ácido é
Ao final, ele obteve um suco com concentração hidrogeniônica de
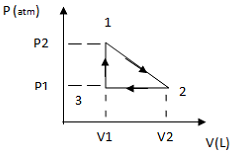
Fonte: FUNCERN, 2015
Com base nas informações do gráfico,
• dobrando a concentração de A, a velocidade de formação de C duplica; e
• dobrando a concentração de B, a velocidade de reação de C quadruplica.
Com base nessas informações,
I) CO2(g) → C(grafite) + O2(g) ΔH1 = 94 kcal
II) H2(g) + 1/2O2(g) → H2O(l) ΔH2 = – 78 kcal
III) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔH3 = – 222 kcal
IV) C(grafite) + 2H2(g) → CH4(g) ΔH4 = ?
Com base nessas informações,
A massa de bórax necessária para preparar 1L de uma solução a 0,1mol/L é
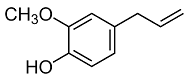
Fonte: FUNCERN, 2015.
Com base nessas informações, é correto afirmar que o eugenol possui
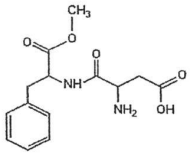
Fonte: FUNCERN, 2015.
Sabendo que a fórmula molecular da sacarose é C12H22O11, a quantidade de sacarose que corresponderá a 5 g de aspartame é
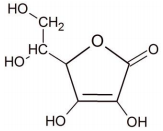
Fonte: FUNCERN, 2015.
Sabendo que um comprido efervescente contém 1 g desta vitamina, a relação entre a quantidade ingerida de vitamina C e a quantidade indicada para ingestão é