Questões de Concurso Sobre química
Foram encontradas 13.580 questões
I – Os raios catódicos são atraídos por uma chapa metálica ligada ao polo positivo de uma bateria.
II – A mudança dos gases no interior dos tubos não afeta a razão carga/massa dos raios catódicos.
III – A razão carga/massa dos raios canais é dependente do gás presente no interior das ampolas.
IV – Ao inverter a ligação dos polos da fonte com os eletrodos das ampolas, os raios catódicos se transformam em prótons.
Estão corretas APENAS as afirmativas
I – foram pesados 2,22 g de cloreto de cálcio;
II – a massa do sal foi dissolvida em 200 ml de água em um béquer;
III – transferiu-se o conteúdo do béquer para um cilindro graduado, onde se adicionou água até que o volume de solução fosse de 500 ml.
Se 100 ml da solução de cloreto de cálcio foi misturada a 100 ml de uma solução aquosa de cloreto de sódio 5,85 g/L, a concentração de íons cloreto, em mol/L, na mistura, é de
I – É possível formar mais amônia com a pressão de 1,0 atm se a temperatura for menor que 450 K.
II – Na temperatura de 450 K e pressão de 1,0 atm, não há formação de amônia, porque o processo está em equilíbrio.
III – Com a pressão em 1,0 atm e a temperatura de 450 K, é possível formar mais amônia, utilizando um catalisador.
IV – Para formar mais amônia na temperatura de 450 K, é preciso que a pressão seja maior que 1,0 atm. /
São corretas APENAS as afirmativas
• Descora a solução de bromo em tetracloreto de carbono.
• Produtos iguais são formados quando se reage com ácido bromídrico na presença ou não de peróxido.
• Sua fórmula molecular é CnH2n-2
Esse hidrocarboneto é o
I – Adicionando-se HCl(aq) , ocorrerá evolução de H2(g) caso o sólido seja o carbonato de potássio.
II – Adicionando-se Na2S(aq) , ocorrerá precipitação, caso o sólido seja o cloreto de bário.
III – Adicionando-se H2O(l) e borbulhando-se CO2(g) , ocorrerá precipitação, caso o sólido seja óxido de sódio.
IV – Adicionando-se H2SO4(l) , ocorrerá evolução de ácido clorídrico, caso o sólido seja o cloreto de sódio.
Estão corretas APENAS as considerações
2KO2(s) + CO2(g) ? K2CO3(s) + 3/2 O2(g)
Se uma pessoa exala cerca de 1020,0 L de gás carbônico por dia, a quantidade de superóxido necessária para capturar todo o gás carbônico num período de três dias de viagem, em kg, é
Dado: Densidade do gás carbônico = 1,960 g/L
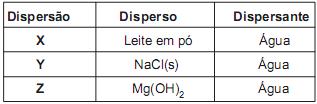
As dispersões X, Y e Z podem ser classificadas, respectivamente, como
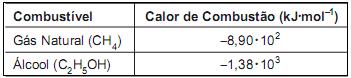
O volume, em litros, de gás natural, medido nas CNTP, que precisa ser queimado para produzir a mesma quantidade de calor que resulta da combustão de 1,0 mol de etanol é igual a
NH4 NO3 (s) -> N2O(g) + 2H2O(g)
As entalpias padrão de formação dos compostos NH4NO3 (s), N2O(g) e H2O(g) são iguais a -365,3 kJmol –1 , +81,6 kJmol –1 e -241,8 kJmol –1 , respectivamente. Sendo ΔH0 , ΔS0 e Δ?G0 , respectivamente, as variações de entalpia, entropia e energia livre padrão para a reação, a decomposição do nitrato de amônio em óxido de dinitrogênio e água apresenta
x Cr2O72–(aq) + y H+(aq) + z I1–(aq) ? w Cr3+(aq) + kI2(g) + pH2O(l)
A soma total dos coeficientes estequiométricos mínimos e inteiros x, y, z, w, k e p na equação química balanceada será igual a
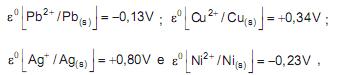
ocorrerá oxidação da lâmina de cobre APENAS na(s) solução(ões) de
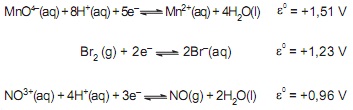
As seguintes afirmações são apresentadas:
I – haverá reação espontânea quando NO(g) for borbulhado em solução aquosa ácida (pH = 0) de KMnO4 1,0 mol L–1 ;
II – haverá reação espontânea quando Br2 (g) for borbulhado em solução aquosa ácida (pH = 0) de KMnO4 1,0 mol L–1 ;
III – o bromo apresenta poder oxidante maior que o de uma solução de ácido nítrico 1,0 mol L–1 ;
IV – uma solução de ácido nítrico 1,0 mol L–1 apresenta poder oxidante maior que o de uma solução aquosa ácida (pH = 0) de KMnO4 1,0 mol L–1 .
Estão corretas APENAS as afirmativas
CO2(g) + H2(g) -> CO(g) + H2O(g) -> ΔH0 = +41,2 KJ.mol –1
Sabendo-se que os calores de formação padrão para H2O(g) e Fe2O3 (s) são iguais a -241,8 kJ×mol –1 e -824,8 kJ x mol –1 , respectivamente, a variação de entalpia no estado padrão para a reação
Fe2O3 (s) + 3CO(g) -> 2Fe(s) + 3CO2 (g)
será igual a

