Questões de Concurso Sobre química
Foram encontradas 13.584 questões
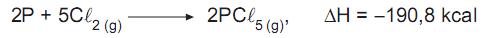
A equação termoquímica acima representa a reação de formação do elemento
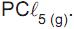 Qual o calor de formação desse elemento?
Qual o calor de formação desse elemento?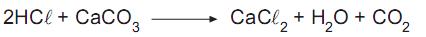
Qual a massa, em gramas, de água que é produzida na reação do ácido clorídrico com 50 g de carbonato de cálcio, conforme o processo químico mostrado acima?
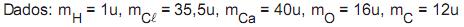

Na reação de oxidação do ferro, mostrada acima, equilibrando-se corretamente a reação no lado esquerdo, qual o número de mols de oxigênio
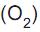 necessário para reagir completamente com uma amostra que contenha 16 mols de Ferro (Fe)?
necessário para reagir completamente com uma amostra que contenha 16 mols de Ferro (Fe)?
Considerando-se que o grau de dissociação do
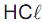 é de 30% e que no equilíbrio existe 1,4 mol de
é de 30% e que no equilíbrio existe 1,4 mol de 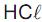 , qual o valor de n?
, qual o valor de n?
Qual o valor da constante de equilíbrio, em (mol/L) -2 , para esse sistema?
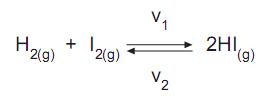
A reação química entre o iodo e o hidrogênio é uma reação reversível, que produz iodeto de hidrogênio. A velocidade de reação direta é
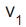 e a velocidade de reação inversa é
e a velocidade de reação inversa é 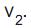 Qual a característica que se estabelece ao atingir o equilíbrio químico no sistema acima?
Qual a característica que se estabelece ao atingir o equilíbrio químico no sistema acima?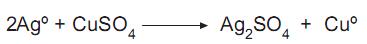
Na reação química acima, a prata reage com sulfato de cobre, obtendo sulfato de prata e cobre puro. Qual o agente oxidante nessa reação?
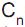 = 0,4 mol/L. Qual é a massa total, em gramas, de NaOH nessa solução?
= 0,4 mol/L. Qual é a massa total, em gramas, de NaOH nessa solução?
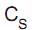 = 180 g/100 g
= 180 g/100 g 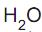 . Qual a massa de água, em gramas, presente numa solução saturada que contenha 36 g desse sal na mesma temperatura?
. Qual a massa de água, em gramas, presente numa solução saturada que contenha 36 g desse sal na mesma temperatura?A tabela a seguir fornece os dados cinéticos obtidos para a reação 2ICl(g) + H2(g) → I2(g) + 2 HCl(g)
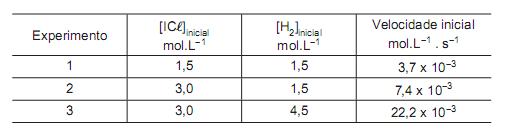
A partir dos dados experimentais obtidos, a expressão da velocidade para essa reação é
LAVOISIER, A.L. Tratado Elementar de Química. São Paulo: Madras, 2007, p. 162.
Já no final do séc. XVIII, Lavoisier utilizou uma linguagem química que nos é muito familiar atualmente. No trecho acima, ele descreve, por exemplo, a reação química entre o carbonato de cálcio (presente no mármore) e o ácido sulfúrico. Essa reação está corretamente representada em
