Questões de Concurso
Comentadas sobre representação das transformações químicas em química
Foram encontradas 778 questões
O nitreto de silício (Si3N4), que é um composto cerâmico que combina diferentes propriedades, como alta resistência mecânica, moderada condutividade térmica e baixo coeficiente de dilatação térmica, tem sido empregado na fabricação de turbinas a gás, peças de motores automotivos e rolamentos e ferramentas de corte de metais. Industrialmente, o composto pode ser preparado por redução carbotérmica em atmosfera de nitrogênio, de acordo com a equação química a seguir.
3SiO2(s) + 6C(s) + 2N2(g) → Si3N4(s) + 6CO(g)
Com base nesse processo, a máxima massa em Kg de nitreto de
silício formada, em quilogramas, quando são colocados para reagir
360,0 kg de SiO2(s), 160,0 kg de C(s) e 140,0 kg de N2(g)
corresponde a
Objetivando estudar a Lei Ponderal de Lavoisier, um estudante realizou o experimento esquematizado a seguir, em que o líquido do frasco A corresponde a uma solução aquosa de ácido sulfúrico (H2SO4) e o sólido contido no frasco B representa uma amostra de carbonato de sódio (Na2CO3).
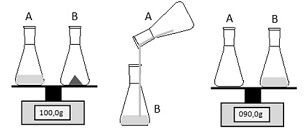
Ao final do processo o estudante notou, pela leitura no visor da
balança, que a massa resultante era diferente da massa inicial. No
contexto do experimento, essa situação foi verificada porque
O processo de extração do ferro é altamente poluente, uma vez que, além da queima de combustíveis fósseis para alimentar os altos-fornos, ocorre a transformação de carvão em monóxido de carbono, conforme ilustrado na reação a seguir envolvendo o minério hematita:
Fe2O3 + 3C → 2Fe + 3CO
Assinale a alternativa que indica a massa de CO produzida no processamento de uma tonelada de hematita. (Pesos atômicos: C = 12, O = 16, Fe = 56.)
A ureia (CO(NH2)2) é uma substância utilizada como fertilizante. Ela pode ser obtida pela reação entre o gás carbônico e amónia, conforme a equação a seguir:
CO2(g) + 2 NH3(g) → CO(NH2)2(s) + H2O(g)
Sabendo-se que 44,8 litros de amónia gasosa reagem completamente em um processo com o gás carbônico, assinale a alternativa que apresenta massa de ureia sólida obtida. (Considerar CNTP).
Nanopartículas esféricas de ouro são estruturas que contêm centenas de átomos de Au. A superfície dessas nanopartículas apresenta carga elétrica advinda de uma camada de íons provenientes do reagente usado na redução do Au3+ para o Au que forma a nanopartícula. A elevada relação superfície-volume e a carga superficial mantêm as nanopartículas dispersas homogeneamente no meio aquoso.
Considerando que cada uma das nanopartículas tenha 100 átomos de Au e que a concentração de Au3+ na reação que originou a dispersão era de 1 x 10-6 mol L-1, o número de nanopartículas de ouro em 5 mL de dispersão aquosa será de
Dado
1 mol de átomos = 6 x 1023 átomos
O clorato de potássio (KClO3), quando aquecido, se decompõe segundo a equação química abaixo.
2 KClO3(s) → 2 KCℓ(s ) + 3O2(g)
Uma mistura com massa desconhecida contém apenas KCℓO3 e KCℓ e foi aquecida produzindo 0,175 mol do gás oxigênio proveniente da reação de decomposição completa do KCℓO3. Após o aquecimento, a massa final de KCℓ foi de 25,0 g.
Dessa forma, a massa total aproximada, em gramas, da mistura que foi aquecida era de
Dados
M(KCℓ) = 75 g mol-1
M (KCℓO3) = 123 g mol-1
Considere as seguintes equações químicas de oxirredução balanceadas a seguir:
Fe2O3(s) + 3 CO(g) → 2 Fe(s) + 3 CO 2(s) (I)
2 K(s) + 2 H2O(ℓ) → 2 KOH(aq) + H2(g) (I)
2 NaBr(aq) + Cℓ2(g) → 2 NaCℓ(aq) + Br2(ℓ) (III)
Em cada uma das equações, o agente oxidante é a espé
cie química:
O tricloreto de fósforo (PCℓ3) é um composto químico muito utilizado como matéria-prima para obtenção de diversos compostos organofosforados. Ele é comumente preparado, sob condições adequadas, de acordo com a equação química balanceada representada a seguir.
P4(s) + 6 Cℓ2(g) → 4 PCℓ3(l)
O valor mais próximo da massa, em gramas, de PCℓ3 que se formaria a partir de 12,4 g de P4 e 30,0 g de Cℓ2, considerando um rendimento de 100%, seria
Dados
M (P4) = 123,9 g mol-1
M (Cℓ2) = 70,9 g mol-1
M (PCℓ3) = 137,3 g mol-1
No processo industrial de soldagem oxi-acetilênica, o acetileno é preparado por uma reação entre o carbeto de cálcio e a água (R1). Além disso, a combustão do acetileno acontece em presença de oxigênio (R2). Considerando que o volume molar dos gases nas condições normais de temperatura e pressão é 22,7L/mol, ajuste os coeficientes estequiométricos e responda:
Qual será a massa de carbeto de cálcio necessária para produzir acetileno e encher um cilindro de 0,05 m3? Qual é a massa de oxigênio necessária para ocorrer a combustão total de 0,05 m3 de acetileno?
Massa atômica Ca= 40, C= 12, O= 16, H= 1 g/mol
CaC2(s) + H2O(I) → C2H2(g) + Ca(OH)2(s) R1
C2H2(g) + O2 → CO2(g) + H2O(g) R2
Num experimento químico eram necessários 60 gramas de iodeto de cobre (I), mas este reagente estava em falta. Assim a solução do problema era fabricá-lo de acordo com a reação química a seguir:
KI(aq) + CuSO4(aq) → I2(s) + K2SO4(aq) + CuI(s)
Quantos gramas de sulfato de cobre (II) serão necessários para formar a quantidade exata de iodeto
de cobre (I)?
Em uma ação policial para combate ao tráfico de substâncias psicoativas (“drogas de abuso”), foram apreendidos 10.000 (dez mil) tubos plásticos, de formato cônico, do tipo eppendorf, com volume de 1,5 mL, cujo interior apresentava sólido pulverizado de coloração bege, que preenchia um volume de 1,0 mL de cada um dos tubos. Durante o exame preliminar do material, foram feitas as seguintes observações:
• Todos os tubos apresentavam as mesmas dimensões e foram preenchidos com o mesmo volume, massa e tipo de pó.
• A massa do material apreendido (correspondente à soma da massa dos tubos e do pó contido em todos os tubos) era de 15.000g (quinze mil gramas).
• A massa de 10 tubos, obtida após a remoção completa do pó de cada um deles, era de 10,0g.
Além disso, por meio de técnicas de amostragem e analíticas, determinou-se que o pó, em todos os tubos, apresentava um teor de cocaína de 5,0%.
O ferro metálico pode ser obtido industrialmente por meio da seguinte reação não balanceada:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Considerando uma reação com transformação
total de produtos em reagentes, assinale a
alternativa correta sobre esse processo.