Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.136 questões
Foi detectada a presença de 32µg de dióxido de enxofre em 100L de ar de um recinto fechado que se encontra a 25°C (a 1 atm).
A composição em ppm (v/v) desse poluente no recinto, considerando o comportamento ideal dos gases, é aproximadamente igual a
Dados: Constante dos gases = 0,082 atm.L.mol–1 .K–1 . Massa molares (g.mol–1 ): S = 32 e O = 16
O nitrogênio amoniacal é um parâmetro relevante para avaliação da qualidade da água e pode ser determinado pelo método de Kjeldahl.
Utilizando esse método, todo o nitrogênio de uma amostra de um efluente foi adequadamente transformado em amônia que foi recolhida em solução de ácido bórico. Posteriormente o borato formado foi titulado, consumindo 24 mL de solução padrão de ácido sulfúrico 0,5 mol.L-1 .
A massa de nitrogênio (em mg) presente na amostra, é aproximadamente igual a
Dados: Massa molares (g.mol-1) H3BO3 = 62, H2SO4 = 98, NH3 = 17 e N = 14.
Um dos critérios que pode ser utilizado para classificar águas naturais é o de dureza, propriedade que resulta da dissolução de minerais do solo e das rochas ou do aporte de resíduos industriais.
A classificação de águas naturais, de acordo com a dureza, é expressa em função da concentração de
Os ciclos biogeoquímicos contribuem para a troca de matéria e energia entre a hidrosfera, a atmosfera e a litosfera.
O ciclo hidrológico está relacionado à distribuição da energia solar assim como as propriedades da água estão relacionadas às seguintes funções:
I. ao transporte de nutrientes no meio aquoso.
II. à alta solubilização de espécies iônicas.
III. à flutuação do gelo e à circulação vertical de nutrientes na coluna d’água.
IV. à estabilização da temperatura da biota.
A água realiza essas funções graças às seguintes propriedades:
Leia o fragmento a seguir.
"Os alquimistas do século XIV tornaram-se os primeiros a compreender a natureza dos ácidos. O único ácido conhecido pelos antigos fora o ácido acético fraco do vinagre. No século VIII, Djabir havia preparado uma solução fraca de ácido nítrico e outros alquimistas árabes descobriram que a destilação do vinagre produzia um ácido acético mais forte. Mesmo o ácido acético forte, porém, pouco tinha de corrosivo. Não parecia ser dotado de muito poder reagente.”
(STRATHERN, P. O sonho de Mendeleiev. A verdadeira história da química. 2002, Zahar, p. 57).
Com relação aos ácidos, assinale V para a afirmativa verdadeira e F para a falsa.
( ) O ácido acético pode ser classificado como forte ou fraco dependendo do valor do seu Ka, o que explica as observações obtidas pelos alquimistas.
( ) O ácido nítrico é um ácido fraco, o que corresponde ao observado experimentalmente pelos alquimistas.
( ) Tanto o ácido acético como o ácido nítrico são ácidos fortes, porém os alquimistas não tinham informações suficientes para classificá-los corretamente.
As afirmativas são, respectivamente,
O conceito de solubilidade pode ser trabalhado em sala de aula por meio de análise da curva de solubilidade apresentada sob a forma de gráficos e/ou da realização de experimentos simples que mostrem os fatores que alteram a solubilidade.
Após uma discussão sobre esse assunto em sala de aula foram levantados pelos alunos alguns fatores que alteram a solubilidade tais como: o solvente, o ponto de fusão do soluto, a temperatura da solução, a pressão, as interações intermoleculares envolvidas.
O fator apresentado pelos alunos que deve ser rediscutido por não influenciar na solubilidade das substâncias é
Leia o fragmento a seguir.
“O objetivo da atividade é evidenciar que esse tipo de transformação envolve a formação de novas substâncias e que podem ser acompanhadas de aspectos facilmente perceptíveis ou evidências.”
(MACHADO, A.H. Aula de Química: discurso e conhecimento. Ed. UNIJUÍ, Ijuí, 3ª ed., 2014.)
Em uma das práticas apresentadas pela autora, os alunos deveriam misturar em um tubo de ensaio três gotas de solução de nitrato de chumbo II e três gotas de bicromato de potássio.
Ao realizar esse experimento, os alunos deveriam observar
sal ΔHsol (kJ/mol) solubilidade em água a 18 ºC (g/100 mL)
LiF +32 0,3
KF +2 92,3
RbF 3 130,6
Considerando os dados na tabela precedente, que lista alguns sais
e seus respectivos valores de entalpia de dissolução (ΔHsol) e
solubilidade, assinale a opção correta a respeito de soluções e
propriedades de soluções.
Texto 19A1BBB
Um caminhão contendo ácido sulfúrico (H2SO4) concentrado tombou e seu conteúdo vazou sobre a rodovia e atingiu um pequeno lago nas imediações. Nos dias que se seguiram ao acidente, a análise da água do lago detectou uma concentração analítica do ácido igual a 1,00 • 10 2 mol/L. Visando-se a neutralizar a acidez causada na água do lago, um produto químico foi utilizado.
Para responder à questão, considere que a solução formada tenha comportamento ideal, que inicialmente a água se encontrava com pH neutro, que a primeira ionização do ácido sulfúrico seja completa e a segunda ionização seja parcial, e assuma 0,30 como o valor de log 2.
Para preparar 500 mL de uma solução de ácido clorídrico, HCl, 6,0 mol/L, um funcionário de um laboratório químico empregou uma solução de ácido clorídrico de concentração 12 mol/L.
O volume do ácido clorídrico 12 mol/L empregado para a preparação da solução 6,0 mol/L foi
Um funcionário de laboratório de análises precisa preparar 1 L de uma solução de hidróxido de sódio, NaOH, massa molar 40 g/mol, com concentração 0,5 mol/L.
Assinale a alternativa que apresenta a massa de hidróxido de sódio que deve ser empregada para o reparo dessa solução.
Considere que em uma amostra de água fluvial foi analisada a concentração de Fe+2 por meio da titulação redox. Para isso retirou-se uma alíquota de 50 mL da amostra da água, que foi titulada com uma solução-padrão de KMnO4 0,10 mol/L em meio ácido.
Se 20 mL da solução de permanganato são necessários para atingir o ponto final da titulação, a concentração de íon ferro (II), em mol/L, na água fluvial, é igual a
Analise a situação a seguir.
Em um preparo de 100 mL de uma solução de ácido clorídrico (HCl) 0,1 mol/L, um técnico retirou da solução estoque 1 mL e completou com água até a linha de aferição.
Considerando que a densidade da solução estoque era 1,1 g/mL, qual a porcentagem aproximada em massa do ácido que estava contida no estoque?
A formação de complexos é usada de muitas maneiras em Química Analítica . A análise química nessa área pode ser utilizada, por exemplo, para medir a quantidade de um analito, para controlar a quantidade efetiva deste que está disponível para outras reações ou como ferramenta para separação de substâncias químicas.
Considerando esse contexto, avalie as seguintes afirmativas e a relação proposta entre elas.
I. A formação de complexos é uma reação na qual ocorre uma ligação reversível entre duas ou mais espécies químicas distintas, como por exemplo, a amônia e Cu2+,
POR QUE
II. nesse caso o NH3 fornece um par de elétrons para os orbitais externos de um íon Cu2+, formando um complexo entre a amônia e o íon metálico, característico de uma reação ácido-base de Lewis.
A respeito dessas afirmativas e da relação proposta entre elas, assinale a alternativa correta.
Os métodos potenciométricos de análises se baseiam na medida do potencial de células eletroquímicas, sem o consumo apreciável de corrente. Há cerca de um século, as técnicas potenciométricas têm sido utilizadas para localizar o ponto final em titulações.
Considere que em uma titulação potenciométrica de 10 mL de ácido clorídrico (HCl), a partir de um padrão de NaOH 0,10 mol/L, os resultados experimentais foram estimados utilizando o método da primeira derivada, conforme descrito no gráfico a seguir.
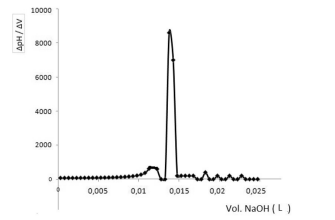
Nesse contexto, a concentração de ácido clorídrico em
mol/L titulado por hidróxido de sódio é igual a
O ponto estequiométrico, de equivalência ou final teórico de uma titulação é aquele calculado com base na estequiometria da reação envolvida na titulação.
Na técnica de volumetria, a solução padrão é a solução cuja concentração é conhecida com exatidão e que estará sendo usada para comparação das concentrações.
