Questões de Concurso
Comentadas sobre substâncias e suas propriedades em química
Foram encontradas 383 questões
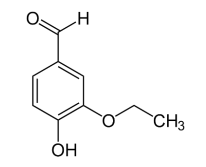
Com base nisso, assinale a alternativa que apresenta as funções químicas encontradas na etilvanilina.
É um lipídio constituído por um álcool policíclico de cadeia longa encontrado nas membranas celulares e no plasma sanguíneo de todos os mamíferos.
Observe a estrutura química apresentada abaixo.
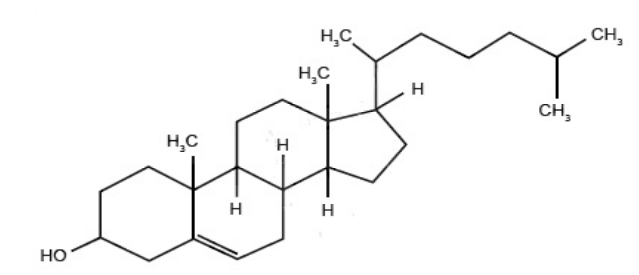
Assinale a alternativa correspondente à fórmula molecular do colesterol.
Considere as massas molares (g.mol-1 ):
Fe2O3 = 159,69; FeSO4 = 151,91; (NH4)2SO4 = 132,14.
A pureza (%) da amostra é, aproximadamente,
Quanto maior o número de partículas na amostra, maior será ______ da radiação incidente e, portanto, menor será a quantidade de radiação incidida no detector.
Assinale a opção que preenche corretamente a lacuna do fragmento acima.
Após a quantificação de rodamina B na amostra, para recuperar o corante em sua forma sólida, será adequado realizar uma destilação simples.
Nos estudos de Alessandro Volta, que tomou como base os experimentos e as teorias de Galvani, foram utilizados diferentes discos de metais (Cu/Sn ou Zn/Ag) empilhados e conectados com pedaços de papel umedecidos em solução salina. Dessa maneira, o cientista conseguiu encontrar o método para a geração de corrente elétrica e estabeleceu evidências para a existência da eletricidade por meio da construção da pilha — cujo nome vem do empilhamento dos discos. Na tabela a seguir, são mostrados os potenciais padrão de redução de algumas espécies químicas em água.

A liga metálica aço inoxidável, material resistente à corrosão, é uma mistura homogênea formada, principalmente, por átomos de ferro e carbono.
Internet: <g1.globo.com> (com adaptações).
Considerando as informações do texto anterior, julgue o item subsequente.
O anidrido bórico é um óxido obtido a partir da retirada total de moléculas de água da estrutura do ácido bórico e possui fórmula molecular BO3.
Internet: <g1.globo.com> (com adaptações).
Considerando as informações do texto anterior, julgue o item subsequente.
O ácido bórico possui geometria trigonal plana em relação ao átomo de boro, e o ângulo observado nas ligações entre esse átomo e os átomos de oxigênio é de 120°.
Internet: <qnesc.sbq.org.br> (com adaptações).
A partir do texto apresentado, julgue o item a seguir.
A tensão superficial observada na água está relacionada às ligações de hidrogênio entre as moléculas, o que causa a impressão de existir uma película fina na superfície do líquido.
Internet: <qnesc.sbq.org.br> (com adaptações).
A partir do texto apresentado, julgue o item a seguir.
As forças de atração tendem a ser mais fortes no estado sólido que no estado líquido, o que faz a velocidade molecular também ser maior nos sólidos que nos líquidos.
Internet: <qnesc.sbq.org.br> (com adaptações).
A partir do texto apresentado, julgue o item a seguir.
A ligação de hidrogênio é a interação intermolecular mais forte que há, por isso a água, mesmo sendo uma molécula de baixa massa molecular, possui elevada temperatura de ebulição.
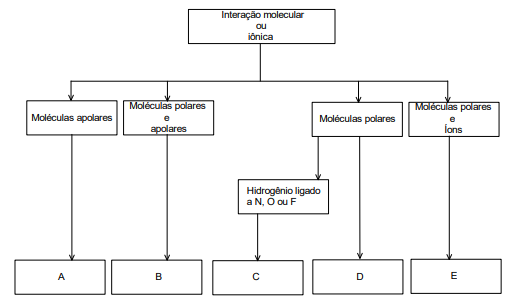
Considerando o fluxograma apresentado, assinale a alternativa que correlaciona corretamente o tipo de ligação intermolecular com as letras A, B, C, D e E, respectivamente.
• antes da separação: massa do vidro de relógio + papel filtro = 62,90 g; • após a separação: massa do conjunto vidro de relógio + papel filtro + areia = 65,65 g.
Diante dessas informações, assinale a alternativa que apresenta corretamente o teor percentual (m/m) de areia nessa amostra.
( ) Átomos que compartilham elétrons para preencher camadas de valência formam ligações covalentes.
( ) As ligações covalentes são classificadas em duas categorias, polares e apolares, dependendo da diferença de eletronegatividade entre os átomos ligados.
( ) Os átomos de elementos com eletronegatividades muito diferentes tendem a formar entre si ligações covalentes.
( ) Na formação do NaCl a partir dos átomos de sódio e cloro, um elétron é transferido da camada de valência do sódio para a camada de valência do cloro.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Após a leitura, assinale a opção que mostra O SOMATÓRIO DOS COEFICIENTES ESTEQUIOMÉTRICOS, expressos com os menores inteiros, da reação citada na etapa 1 acima, A GEOMETRIA MOLECULAR da arsina e o ESTADO DE OXIDAÇÃO (Nox) do arsênio no ácido arsênico, respectivamente:
I. A uma temperatura fixa, uma solução aquosa saturada de um determinado soluto sempre contém uma quantidade fixa desse soluto;
II. Todos os líquidos fervem a uma temperatura superior ao seu ponto de ebulição normal quando contêm impurezas não voláteis;
III. Toda solução comporta-se como uma solução ideal.
Com base na análise dos itens I, II e III, assinale a opção CORRETA: