Questões de Concurso
Sobre substâncias e suas propriedades em química
Foram encontradas 1.458 questões
A separação dos diferentes hidrocarbonetos de petróleo utiliza, como método, a destilação fracionada.
A separação de água e óleo também pode ser feita com o método de dissolução fracionada.
O texto retrata vários tipos de separações físicas da água do mar com o petróleo.
Via de regra, os aços mais dúcteis, largamente utilizados em elementos estruturais e tubulações, são aços:
O processo descrito é um exemplo de:
A técnica que consiste na separação de dois líquidos por meio do aumento da temperatura até atingir o ponto de ebulição de um deles, seguido pela condensação do vapor, é um exemplo de:
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

O fato de o NaCl fundir-se a 801 °C e o MgO fundir-se a 2.852 °C é uma evidência de que os sólidos iônicos são unidos por interações entre cátions e ânions, isto é, ligações iônicas.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Os sólidos iônicos são cristalinos, e os sólidos moleculares são amorfos.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

No gráfico apresentado, o segmento de curva entre os pontos O e T representa a curva de sublimação, que separa a fase sólida da fase gasosa, e cada ponto desse segmento é uma condição de equilíbrio entre o sólido e o gás.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

No gráfico apresentado, os processos indicados pelas setas I e IV representam, respectivamente, os processos de vaporização e congelamento da referida substância.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Nos líquidos, a ordem de ligação tem mais curto alcance que nos sólidos cristalinos.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

As moléculas se organizam por meio de ligações covalentes entre si para formar os sólidos moleculares.
Uma das principais vantagens da teoria de ligação de valência é a possibilidade de explicar, satisfatoriamente, fenômenos associados a estados de excitação e de prever os espectros de absorção e emissão de energia eletrônica das moléculas.
Nos compostos formados por cátions e ânions muito polarizáveis, o caráter da ligação química é fortemente covalente.
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
De acordo com a teoria de ligação de valência, a molécula de água é constituída por quatro orbitais híbridos do tipo sp3 arranjados de forma tetraédrica em torno do oxigênio, de maneira que dois orbitais participam das ligações simples O–H e outros dois acomodam os pares de elétrons não ligantes.
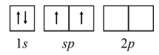
De acordo com a teoria de ligação de valência, o diagrama de orbitais para o átomo de Be, para formar orbitais híbridos no BeF2, está corretamente representado na figura a seguir.
O comprimento da ligação entre o hidrogênio e o átomo de halogênio é maior no HI que no HF.