Questões de Concurso
Comentadas sobre transformações químicas e energia em química
Foram encontradas 366 questões
O Cloreto de alumínio sólido é um ácido de Lewis muito utilizado nas reações de substituição orgânica.
O valor da entalpia padrão de formação deste ácido de Lewis encontra-se entre:
Dados:
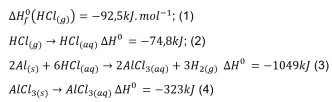
(Fonte: ATKINS, Peter; JONES, Loretta; LAVERMAN,
Leroy. Princípios de Química: Questionando a Vida
Moderna e o Meio Ambiente. Bookman Editora, 2018)
Considere os potenciais padrões de redução apresentados abaixo:
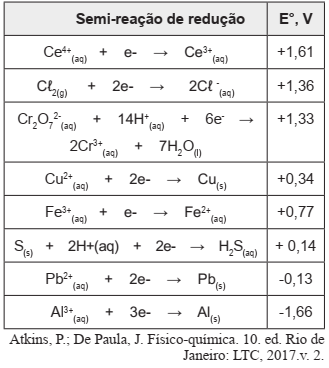
Identifique nas reações abaixo, a que é classificada
como um processo espontâneo.
Corrosão eletroquímica de um metal é um processo que envolve reações redox espontâneas, como exemplo, a indesejada ferrugem. Esta é originada do processo corrosivo do ferro. Um procedimento para evitar a corrosão é a adição de um metal de sacrifício para ser ______________ preferencialmente por apresentar um ___________ potencial de ____________.
Assinale a alternativa que completa o texto acima corretamente.
Considere os valores de entalpia padrão de formação de alguns compostos químicos apresentados na tabela a seguir.

Com base nas informações apresentadas, a variação de
entalpia, em kJ, para a reação de combustão completa de
um mol do gás propano (C3H8) é, aproximadamente:
A respeito das emissões radioativas, julgue o item subsequente.
Em reatores nucleares, a fissão nuclear ocorre com a partição de núcleo atômico pesado e instável em núcleos menores, liberando uma grande quantidade de energia.
A respeito das emissões radioativas, julgue o item subsequente.
A emissão gama apresenta alto poder de penetração, pois possui comprimentos de onda menores, sendo detida por placas de chumbo ou por grossas paredes de concreto.
A respeito das emissões radioativas, julgue o item subsequente.
Partículas alfa apresentam carga elétrica negativa e massa desprezível, enquanto partículas beta são constituídas de dois prótons e dois nêutrons.
A respeito das emissões radioativas, julgue o item subsequente.
Radioatividade é a capacidade que certos átomos
possuem de emitir radiações eletromagnéticas e
partículas de seus núcleos instáveis.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
A eletricidade pode ser usada para fazer com que ocorram reações de oxirredução não espontâneas; na eletrólise, uma reação é levada à direção não espontânea pela passagem de uma corrente elétrica através da solução.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
Em uma pilha galvânica, uma reação química é realizada, utilizando‐se corrente elétrica para sua ocorrência, de forma que a voltagem necessária é a subtração entre os potenciais de redução dos reagentes envolvidos.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
A produção de metais a partir de seus minérios é um processo eletroquímico constituído por reações de oxirredução, sendo esse evento um processo espontâneo realizado em indústrias siderúrgicas.
Com relação às aplicações da química e aos processos eletroquímicos, julgue o item que se segue.
A substância capaz de promover a redução de outra substância é denominada de agente redutor, enquanto a substância responsável pela oxidação de outra substância é denominada de agente oxidante.
Julgue o item a seguir, relativo à termoquímica e a assuntos correlatos.
A entalpia de uma reação é a soma das entalpias de qualquer sequência de reações (na mesma temperatura e pressão) na qual a reação total pode ser dividida.
Assim, a variação de entalpia para qualquer processo depende somente da natureza dos reagentes e dos produtos e independe do número de etapas do processo
ou da maneira como é realizada a reação.
Julgue o item a seguir, relativo à termoquímica e a assuntos correlatos.
As reações químicas são acompanhadas de liberação ou absorção de energia. Se a energia dos produtos é maior que a dos reagentes, a energia é liberada; se a energia dos produtos é menor que a energia dos reagentes, o sistema absorve a energia das vizinhanças durante o curso da reação. Isso está de acordo com a lei da conservação de energia.
Julgue o item a seguir, relativo à termoquímica e a assuntos correlatos.
A quantidade de calor absorvida por um sistema é um número positivo quando o sistema absorve calor das vizinhanças (processo endotérmico). Quando o fluxo de calor está na direção oposta, o sistema perde calor para
as vizinhanças e a quantidade de calor absorvida pelo sistema é um número negativo (processo exotérmico).
Julgue o item a seguir, relativo à termoquímica e a assuntos correlatos.
A termoquímica refere‐se ao estudo das transferências de calor que ocorrem durante as transformações químicas.
Tendo em vista que a inclusão de marcadores fotoluminescentes em munição livre de chumbo faz que o disparo de munição marcada dessa maneira produza resíduos luminescentes facilmente identificáveis na presença de luz ultravioleta, julgue o item subsequente, relacionado ao fenômeno de fotoluminescência envolvido nessa aplicação.
A fosforescência é um processo fotofísico lento, pois envolve uma transição radioativa entre estados de mesma multiplicidade.
A seguir são apresentadas informações referentes à reação de decomposição do H2O2.


Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1 , julgue o item subsequente, acerca da reação em questão.
As entalpias padrão de ligação fornecidas permitem determinar que a decomposição de 1,00 mol de H2O2, quando realizada à pressão constante de 1 bar e a 25 ºC, libera quantidade de calor superior a 100 kJ.
A seguir são apresentadas informações referentes à reação de decomposição do H2O2.


Considerando que a reação de decomposição do H2O2 seja exotérmica e se processe de acordo com uma cinética de primeira ordem, e que a constante universal dos gases seja igual a 8,3 J × mol-1 × K-1 , julgue o item subsequente, acerca da reação em questão.
A reação de decomposição do H2O2 libera maior quantidade de calor quando é realizada à pressão constante de 1 bar do que quando é realizada a volume constante.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Se, na queima de um artefato pirotécnico ocorrera decomposição do carbonato de bário, de acordo coma reação química BaCO3(s) → BaO(s) + CO2(g), entãoa entalpia padrão dessa reação de decomposição (ΔHx),calculada a partir dos dados listados na tabela seguinte,será ΔHx = ΔH1 - ΔH2 + ΔH3.