Questões de Química - Transformações Químicas e Energia para Concurso
Foram encontradas 1.424 questões

Com referência à célula galvânica descrita, considerando que as soluções envolvidas apresentam comportamentos ideais e que log 5 = 0,7 e log 2 = 0,3, julgue os itens seguintes.
 não varia no intervalo de temperaturas entre 373 K e 400 K.
não varia no intervalo de temperaturas entre 373 K e 400 K.Com referência à situação hipotética descrita acima, julgue os itens.

As associações corretas são

Com base nessas informações, julgue os itens que se seguem.
Caso, na reação acima, a coloração amarela torne-se mais intensa ao se aumentar a temperatura do sistema, é correto concluir que a reação será endotérmica no sentido da formação de
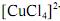 .
. 
Considerando as informações acima e que todos os gases envolvidos sejam ideais, julgue os itens a seguir.
Na equação abaixo, se expressa, corretamente, a quantidade de calor (q) necessária para elevar, a pressão constante, a temperatura de um mol de
 de 298 K até uma temperatura
de 298 K até uma temperatura