Questões de Concurso
Comentadas sobre transformações químicas em química
Foram encontradas 540 questões
2KNO3(s) + S(s) + 3C(s) -> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
A redução do nitrato, que consome três moles de elétrons por mol de NO3 – em meio ácido, gera o óxido nítrico, que é um agente complexante mais forte que o íon nitrato
2KNO3(s) + S(s) + 3C(s) -> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
Se o gás carbônico reagir com a água para formar o ácido carbônico, o CO2 receberá um par de elétrons da água, que é uma base de Lewis.
2KNO3(s) + S(s) + 3C(s)-> K2S(s) + N2(g) + 3CO2(g).
Com base nessas informações, julgue o item seguinte.
O nitrato reage com a água conforme a reação NO3 – + H2O -> 6 HNO3 + OH– , aumentando significativamente o pH da solução formada, haja vista que o caráter básico do OH– é mais forte que o caráter ácido do NO3 – .
O nitroprussiato de sódio — Na2[Fe(CN)5NO] — é um
composto empregado como fonte de óxido nítrico — um potente
vasodilatador — administrado por via intravenosa em pacientes em
situação de emergência hipertensiva. O uso inadequado desse
medicamento, que é sensível à luz e que produz cianeto em sua
decomposição, pode causar morte acidental por déficit de oxigênio
no organismo.
Com base nas informações apresentadas, julgue o próximo item.
Considere que esse complexo é octaédrico e de spin baixo.
Nesse caso, é correto afirmar que existem três elétrons
desemparelhados nos orbitais dxy, dyz e dxz do metal e que há
dois possíveis isômeros para esse complexo
O nitroprussiato de sódio — Na2[Fe(CN)5NO] — é um
composto empregado como fonte de óxido nítrico — um potente
vasodilatador — administrado por via intravenosa em pacientes em
situação de emergência hipertensiva. O uso inadequado desse
medicamento, que é sensível à luz e que produz cianeto em sua
decomposição, pode causar morte acidental por déficit de oxigênio
no organismo.
Com base nas informações apresentadas, julgue o próximo item.
De acordo com a teoria do campo ligante, pelo menos três elétrons ocupam os orbitais t2g não ligantes.
A transformação de carbonato de cálcio em óxido de cálcio pode ser representada pela equação a seguir:
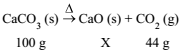
A massa, em gramas, correspondente a X é igual a
Considere as seguintes representações para átomos: 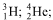
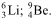 O número de nêutrons de cada átomo é, respectivamente,
O número de nêutrons de cada átomo é, respectivamente,
Dados: massas molares (g.mol -1 ),
H=1, C=12, Cl=35,5, Br=80
Dado: massa molar do Al =27g.mol -1
Dados:
constante de Rydberg (R)= 2,18.10-18 J,
constante de Planck (h)= 6,67.10-34 J.s, velocidade da luz (c)= 3,00.108 m.s-1
A configuração eletrônica desse íon, segundo o diagrama de Pauling, tem como subnível mais energético, Dados: Número atômico do ferro = 26
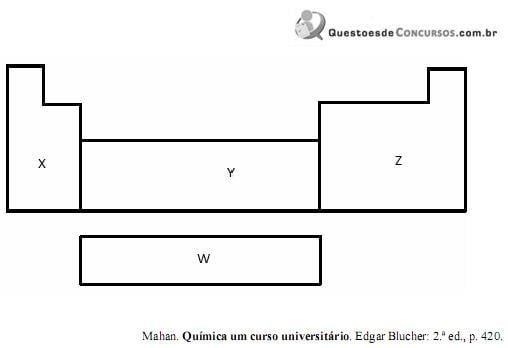
A tabela Periódica pode ser dividida em grupos de elementos, de acordo com o preenchimento dos orbitais de valência. Nesse contexto, as regiões X, Y, Z e W da tabela mostrada acima relacionam-se com o preenchimento dos orbitais de valência


Com relação ao assunto abordado nos textos, assinale a opção correta.
A partir das informações precedentes, e considerando MH2O= 18 g/mol, julgue o item que se segue.
Considere-se que a combustão completa do n-heptano seja processada de acordo com a equação a seguir.
C7H16 (l) + 11 O2 (g) → 7 CO2 (g) + 8 H2O (l)
Considere-se, também, que a constante universal dos gases
ideais seja igual a 0,082 atm∙L∙mol−1∙K−1, que as condições
normais de temperatura e pressão (CNTP) correspondam à
temperatura de 0 °C e à pressão de 1 atm e que o volume
molar de um gás ideal nas CNTP seja 22,4 L. Nessa situação,
para a completa combustão de 44,8 L de n-heptano nas
CNTP, será necessário um volume de O2 superior a 500 L.
A respeito de gases reais, de gases ideais e do modelo cinético dos gases, julgue o item.
A densidade dos gases, em geral, em condições normais
de temperatura e pressão, é menor que a densidade de
líquidos e sólidos.
Na seguinte figura, o recipiente da esquerda tem volume V, pressão P, temperatura T e contém 84 gramas de uma gás ideal. O recipiente da direita, também de volume V, contém 96 g de gás oxigênio puro, também ideal, na pressão P e temperatura T. Com base nessas informações, o gás contido no recipiente da esquerda é o