Questões de Concurso
Comentadas sobre transformações químicas em química
Foram encontradas 515 questões
( ) Sommerfeld propõe que a energia do elétron seria determinada pela distância em que ele se encontra do núcleo e pelo tipo de órbita que descreve.
( ) Hantaro Nagaoka, em 1903, sugeriu um modelo atômico formado por pares de cargas positivas e negativas, aos quais chamou de “dinamidas”. E estes pares de cargas ficariam em blocos flutuantes no espaço.
( ) Em 1904, Philipp Lénard publicou no Japão uma descrição do carbono, bem moderna para época, ele sugeriu que o átomo era constituído de um anel de elétrons ao redor de um centro muito denso.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
I. O físico inglês J. J. Thomson, em 1887, mostrou que as partículas em raio catódico são carregadas negativamente e ele provou esta afirmação mostrando que o raio pode ser desviado se passar entre placas de metais carregados opostamente em um tudo de Crookes. Segundo suas pesquisas, a direção do desvio para a placa carregada positivamente, mostra que as partículas do raio catódico carregam uma carga elétrica negativa.
II. Segundo os pesquisadores dos modelos atômicos, foi no ano de 1908, que Robert Millikan, um físico americano realizou, um clássico experimento, que foi capaz de determinar a magnitude da carga negativa do elétron. Millikan acreditava que os raios x chocavam-se com os elétrons das moléculas do ar que circundavam as gotículas de óleo e que as gotículas poderiam captar estes elétrons. Através de seus experimentos, Milikan foi assim capaz de mostrar que todos os elétrons são idênticos, isto é, todos têm a mesma massa e carga.
III. Embora para a maioria dos cientistas da época o fato do átomo ser constituído por uma parte carregada positivamente e por alguns elétrons, em 1890, isto ainda não era totalmente claro. Em 1898, que J. J. Thomson sugeriu que um átomo poderia ser uma esfera carregada positivamente na qual alguns elétrons estão incrustados. Segundo ele, isto levaria a uma impossível remoção de elétrons dos átomos.
Estão corretas as afirmativas:
HCl + Al(OH)3 → X + Y Ácido Hidróxido de Clorídrico Alumínio
Assinale a alternativa correta quanto aos produtos X e Y.
Adaptado. Disponível em: https://mundoeducacao.uol.com.br/quimica/atomo.htm#:~:text=O%2 0%C3%A1tomo%20%C3%A9%20a%20unidade,explicar%20o%20f uncionamento%20da%20mat%C3%A9ria. Acesso: 06/04/2023.
Observe o quadro abaixo:
1. Modelo do Pudim de Passas ( ) Partícula alfa (radioatividade) 2. Modelo da Bola de Bilhar ( ) Eletrólise (eletricidade) 3. Modelo Planetário (Sistema Solar) ( ) Massas (Leis Ponderais)
Neste contexto, marque a sequência correta entre o Modelo Atômico e os experimentos/ temas científicos realizados.
Adaptado. Disponível em: https://brasilescola.uol.com.br/o-quee/quimica/o-que-e-atomo.htm. Acesso: 06/04/2023.
Com relação aos modelos atômicos, assinale a alternativa correta.
I. Todos os elementos da tabela periódica foram forjados nos processos de vida e morte das estrelas. II. A composição do universo muda continuamente em decorrência do ciclo de vida das estrelas. III. Os elementos químicos que serão produzidos no decorrer do ciclo de vida de uma estrela dependem da massa da estrela.
Estão corretas as afirmativas:
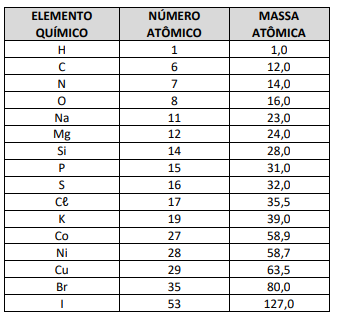
Ventura, D. O lendário azul da Prússia, cor que pode salvar ou tirar vidas. Disponível em www.bbc.com. Adaptado.
A distribuição eletrônica na valência do par associado à conversão eletroquímica de oxidação mencionada no texto é descrita por:
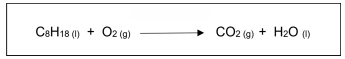
Para queimar completamente 2,00 mols de octano, serão necessários:
Fonte: BBC Brasil, 2023. Disponível em: https://www.bbc.com/portuguese/articles/c7246ee619qo
Em relação às características físico-químicas e ambientais do mercúrio, podemos afirmar que:
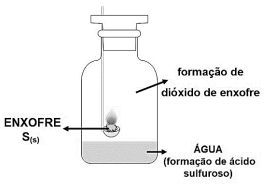
Certa quantidade de enxofre é inserida no dispositivo de combustão e a chama é iniciada no bico de Bunsen. Então, ainda com a chama acesa, o dispositivo é inserido em um frasco hermeticamente fechado e o dióxido de enxofre formado fica confinado no recipiente. Este gás, por sua vez, reage com a água contida no fundo do frasco, formando uma solução de ácido sulfuroso. Considerando todas as informações apresentadas e a imagem, a reação que expressa corretamente a formação do ácido sulfuroso é:
A respeito de estequiometria, processo de fabricação, corrosão e soldagem, julgue o item a seguir.
Considere-se que a reação para a produção de biodiesel ocorra a partir de 1 mol de triglicerídeo (TRIG) e 3 mols de metanol (MET), na presença de um catalisador (NaOH), para formar monoésteres de ácidos graxos (BIO = biodiesel) e 1 mol de glicerina (GLI), conforme a equação que se segue.
1 TRIG + 3 MET → BIO + 1 GLI
Com base nessa hipótese e considerando-se a massa molar
do metanol igual a 32 g/mol e a massa molar da glicerina
igual a 60 g/mol, é correto afirmar que, se forem utilizados
960 kg de metanol na presença de um excesso de
triglicerídeos, para um rendimento de 80% a massa
resultante de glicerina será de 480 kg.
Julgue o item seguinte, referentes ao estudo dos gases.
Os gases diferem de líquidos e sólidos, pois o volume de
uma amostra de gás depende fortemente de sua temperatura e
da pressão que lhe é aplicada. Experimentalmente,
descobriu-se que todos os gases comuns se comportam
aproximadamente da mesma maneira, sendo esse
comportamento descrito pelas leis dos gases. Assim, para
quase todos os gases, o volume de uma amostra de gás a
temperatura constante é inversamente proporcional à
pressão.
Julgue o item seguinte, referentes ao estudo dos gases.
A investigação da relação entre o volume e a temperatura de
um gás mostra que gases sofrem contração quando sujeitos a
um aumento significativo de temperatura. Quando a pressão
e a quantidade de matéria de um gás são mantidas
constantes, o volume desse gás é inversamente proporcional
à temperatura.