Questões de Concurso
Comentadas sobre velocidade de reação, energia de ativação, concentração, pressão, temperatura e catalisador em química
Foram encontradas 139 questões
I. A velocidade de uma reação depende da concentração, mas a constante de velocidade não depende dela.
II. Quanto mais baixa for a energia de ativação, mais lenta a reação.
III. Se a velocidade de aparecimento de O2(g), 2 O3(g) → 3 O2(g), é 9 x 10–4 mol/L em determinado instante, a velocidade de desaparecimento do O3(g) é 18 x 10–4 mol/L.
Está correto o que se afirma em
A equação química abaixo representa a síntese do íon triiodeto.
S2 O82- (aq) + 3 I- (aq) → 2 SO42- (aq) + I3 - (aq)
A fim de descobrir a ordem da reação, três experimentos foram realizados, e os resultados encontrados estão na tabela a seguir. Analise os dados da tabela e assinale a alternativa que possui a ordem desta reação.
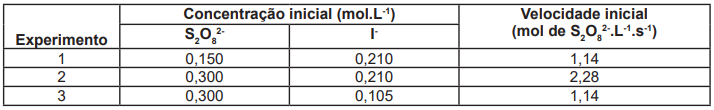
De acordo com os dados apresentados, a lei de velocidade para a reação estudada é:
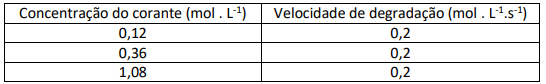
Os dados experimentais apresentados na tabela sugerem uma lei cinética de degradação de ordem:
No que se refere à modificação de superfícies, julgue o seguinte item.
A funcionalização de superfícies antimicrobianas é uma
tecnologia que pode ser utilizada para desinfecção em vários
ramos da atividade humana, por exemplo, na esterilização de
dispositivos médicos para prevenir infecções hospitalares.
Julgue o item que se segue, acerca de modificações de superfícies de biomateriais com proteínas.
Todos os métodos de modificação de superfícies de
biomateriais são essencialmente métodos químicos.
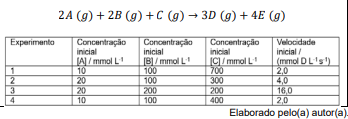
Dada a reação hipotética:

A partir de dados experimentais, verifica-se que o composto A é um reagente de terceira ordem e a substância B é um reagente de primeira ordem da reação.
Se duplicarmos as concentrações dos reagentes A e B, a
velocidade dessa reação aumentará:
Sobre essa lei conclui-se que, para uma reação em meio gasoso, a constante de velocidade
Em uma síntese industrial, o HBr é produzido a partir da seguinte reação química:
H2 (g) + Br2 (g) → 2 HBr (g)
No início da síntese, a concentração de H2
era de 0,3 mol/L.
Após 20 minutos, sua concentração passou a 0,1 mol/L.
Nesse intervalo de tempo, a velocidade média de formação de HBr, em mol L-1
min-1
, correspondeu a
No gráfico abaixo estão representados os caminhos de uma reação com catalisador e uma sem catalisador.
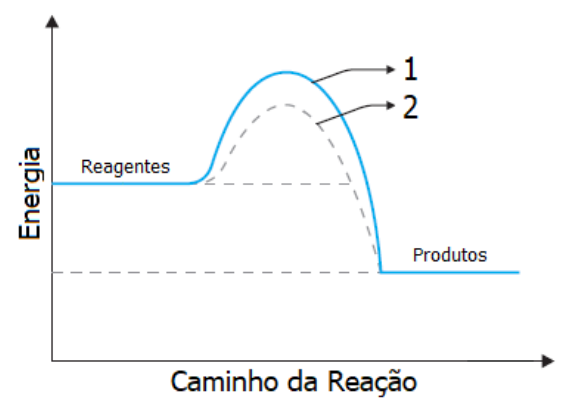
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ) com base nesse gráfico.
( ) A curva 1 refere-se à reação não catalisada e a curva 2 refere-se à reação catalisada.
( ) A energia de ativação da curva 1 é maior do que a da curva 2.
( ) A utilização de um catalisador na reação aumenta o valor de ∆H.
( ) O complexo ativado da curva 1 apresenta a mesma energia do complexo ativado da curva 2.
( ) Se a reação seguir o caminho da curva 2, ela será mais rápida.
Assinale a alternativa que indica a sequência correta,
de cima para baixo.
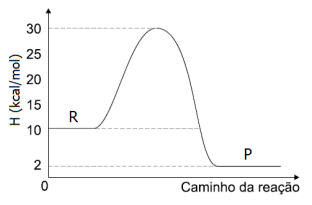
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ) com as informações fornecidas pelo gráfico.
( ) A energia dos reagentes é igual a 30 kcal/mol e a dos produtos é igual a 2 kcal/mol.
( ) O gráfico representa uma reação exotérmica onde são liberadas 8 kcal/mol de energia.
( ) A energia de ativação da reação é igual a 30 kcal/mol e a energia do complexo ativado é igual a 10 kcal/mol.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
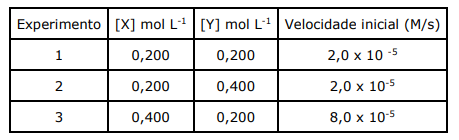
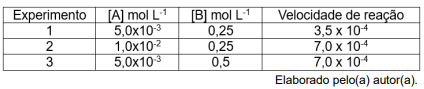
Com base nos dados da tabela, analise as assertivas abaixo:
I. A lei de velocidade para a reação é v= k [X]2 .
II. A concentração de Y não tem nenhum efeito sobre a velocidade da reação.
III. A ordem global da reação é 3.
IV. A constante de velocidade da reação é 2,0 x 10-3 M-1s-1.
Quais estão corretas?
Tabela: Dados obtidos na investigação cinética (método da velocidade inicial) para a reação: 2 A2B(g) → 2 A2(g) + B2(g).
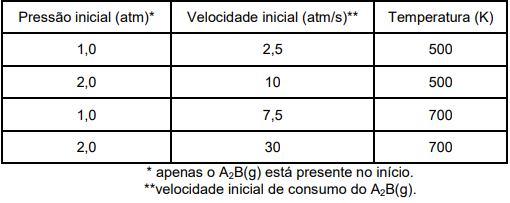
Diante das informações acima, assinale a opção que mostra A VELOCIDADE DA REAÇÃO (em termos de consumo do A2B(g)), em atm/s, quando a pressão de A2B(g) é igual a 1,5 atm à temperatura de 600 K:
Figura: Dados cinéticos para uma reação de primeira ordem. Concentração versus tempo e velocidade versus tempo.
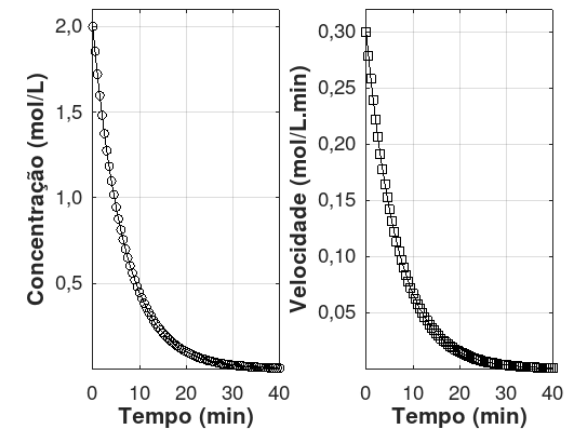
A partir da interpretação dos gráficos mostrados acima, assinale a opção que mostra corretamente O VALOR DO TEMPO DE MEIA-VIDA do processo, em minutos, com precisão de duas casas decimais: Dado: considere ln(2) = 0,693.
O NO produzido na estratosfera pela reação do N2O com o átomo de oxigênio participa da destruição do ozônio na atmosfera.
O NO produzido reage com o ozônio abstraindo um átomo de oxigênio, produzindo o NO2.
Para determinar a expressão da velocidade da reação do NO com o ozônio foram realizados em laboratório, experimentos cujos dados estão na tabela a seguir.
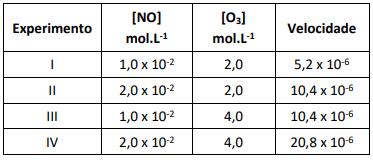
De acordo com os dados, assinale a expressão que descreve a lei da velocidade da reação.
Os catalisadores promovem reações