Questões de Concurso Público CEFET-MG 2022 para Técnico Laboratório - Área Química
Foram encontradas 20 questões
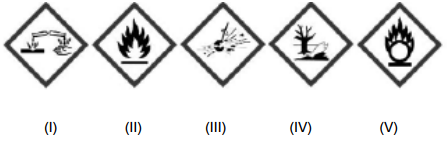
SUBSTÂNCIAS ( ) oxidantes ( ) explosivas ( ) corrosivas ( ) nocivas ao meio ambiente ( ) inflamáveis
A sequência correta é
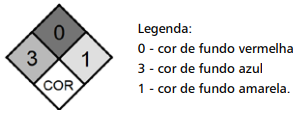
Considerando a representação acima, o técnico de laboratório fará uma leitura correta do risco químico se interpretar que o resíduo é
classe A: Fogo em materiais combustíveis sólidos, que queimam em superfície e profundidade por meio do processo de pirólise, deixando resíduos.
classe B: Fogo em líquidos e/ou gases combustíveis ou inflamáveis e sólidos combustíveis que se liquefazem por ação do calor, como graxas, que queimam somente em superfície, podendo ou não deixar resíduos.
classe C: Fogo em materiais, equipamentos e instalações elétricas energizadas.
classe D: Fogo em metais combustíveis, como magnésio, titânio, alumínio, zircônio, sódio, potássio e lítio.
classe K: Fogo em óleos e gorduras, animais e vegetais, utilizados na cocção de alimentos.
Existem vários tipos de extintores e a utilização de cada um deles depende da classe do incêndio. Os extintores de incêndio com carga de água são indicados principalmente para combater incêndios da(s)
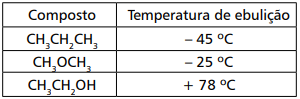
A maior temperatura de ebulição do etanol em comparação aos demais é justificada pelo(a)
Dados: MMFe = 56 g mol-1 MMO = 16 g mol-1
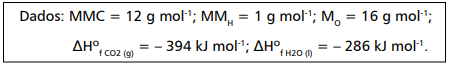
Considerando essas informações, o calor de formação estimado para a glicose, em kJ mol-1, é
HbH+ + O2 →← HbO2 + H+ ∆H < 0
A liberação de gás oxigênio para os tecidos é favorecida pelo(a)
Dados: MMCu = 63,5 g mol-1 / Constante de Faraday = 96500 C
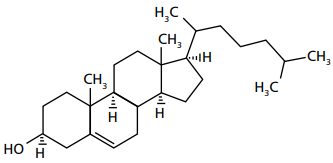
Sobre a estrutura acima, analise se as afirmativas são verdadeiras (V) ou falsas (F):
( ) Apresenta a função fenol. ( ) Apresenta isomeria óptica. ( ) Possui quatro centros de quiralidade. ( ) Possui baixa solubilidade em água. ( ) É um composto meso.
A sequência correta é
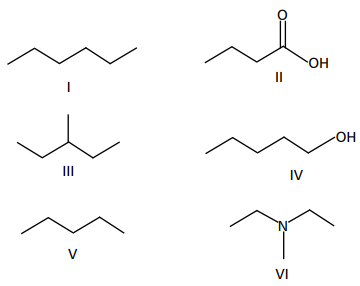
Em relação às propriedades físico-químicas dos compostos, é INCORRETO afirmar que
SO3(g) +H2SO4(l) → H2 S2 O7(l) (Equação1) H2S2O7(l) + H2O(l) → 2H2 SO4(l) (Equação2)
CAMPOS, R. V. Ácico Sulfúrico. Rev. Virtual Quim. 2011, 3(3), 210-214 (adaptado).
Para a produção do ácido sulfúrico 98% m/m, a indústria partiu de 800kg de SO3 e 980kg de H2SO4, além de água o suficiente para obtenção desse produto. A massa de ácido sulfúrico 98% m/m que se pode obter, em kg, é
Dados: Massa molar: O=16g/mol; H=1g/mol; S=32g/mol
DBS (fa) + AM (fa) →← DBS-AM (fo) (Equação 1) DBS-AM (fo) + CB (fa) →← DBS-CB (fo) + AM (fa) (Equação 2)
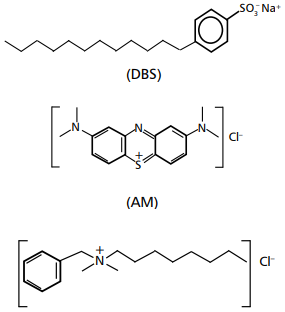 (CB)
(CB) Com base nas estruturas químicas e sabendo-se que o ponto final da titulação se dá quando a fase aquosa e a orgânica apresentam a mesma tonalidade de azul, é correto afirmar que o
HARRIS D. C. Análise Química Quantitativa. 6ª edição. Rio de Janeiro: LTC, 2005.
Durante estudo sobre erro do indicador, o analista fez uma titulação de 10,00mL de Ácido fraco (HA) 0,100mol/L (pka = 4,8) com NaOH 0,100mol/L e obteve um volume final de 9,80mL de base. O quadro abaixo apresenta três indicadores e suas faixas de viragem.
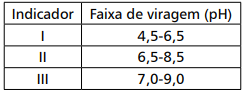
Para que o analista tenha observado esse ponto final, o(s) indicador(es) utilizado(s) foi/foram apenas
Dados: Log 49 = 1,7
Dados: Log 9,9 = 0,99
Dados: Kb(NH3)= 2x10–5
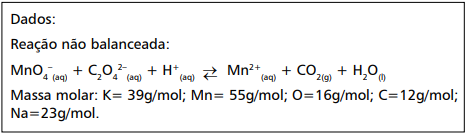
A molaridade dessa solução de KMnO4 é