Questões de Concurso Público Transpetro 2023 para Profissional Transpetro de Nível Superior - Junior: Ênfase 26: Engenharia Química
Foram encontradas 70 questões
I - A cavitação ocorre sempre que o número de Reynolds exceder 200000.
II - A cavitação pode ocorrer no escoamento de líquidos em situações nas quais a pressão local é inferior à pressão de vapor do líquido.
III - As bolhas formadas na cavitação aumentam a resistência local à corrosão.
IV - As bolhas formadas na cavitação colapsam quando atingem regiões nas quais a pressão local é superior à pressão do vapor.
São corretas APENAS as afirmações
Com essas informações, constata-se o seguinte:
Considere a Figura abaixo, que indica uma possível instalação para testes de escoamentos:
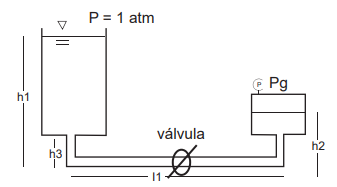
A válvula está fechada, e, nessa situação, não há escoamento. Pg é a pressão manométrica no ponto indicado do reservatório fechado da direita. A área da superfície livre do reservatório da esquerda é muito grande.
Sabendo-se que h1 = 7m; h2 = 1m; h3 = 4m e l1 = 100m;
g = 10 m/s2
e que a massa específica do fluido é igual a
1000 kg/m3
, Patm = 100 kPa, após a abertura da válvula, o
escoamento irá acontecer
Com relação às radiosidades das faces superior e inferior, verifica-se que
NÃO é adequado para essa finalidade o
2 NO2 (g) + ½ O2 (g) + H2 O (g) ⇌ 2 HNO3 (g)
Considere que a reação foi simulada em laboratório, num reator com êmbolo, cujo volume e aquecimento podem ser variados.
É possível deslocar o equilíbrio para formar mais HNO3 , quando
Com base nesse experimento e nas informações fornecidas, a velocidade de reação, v, é expressa pela relação
Cr(OH)3(s) ⇌ Cr3+ (aq) + 3OH- (aq); Kps = 10-30 Cr(OH)3(s) + OH- (aq) ⇌ Cr(OH)- 4 (aq); Ks = 10-0,4
Considerando-se a concentração analítica de cromo de 0,010 mol L-1 , conclui-se que o cromo estará quantitativamente
Sobre essa lei conclui-se que, para uma reação em meio gasoso, a constante de velocidade