Questões de Concurso Público UNEMAT 2024 para Químico
Foram encontradas 25 questões
Considere a reação química representada pelo seguinte equilíbrio químico:
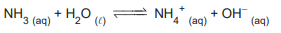
De acordo com a teoria ácido-base de Brönsted-Lowry,
nas reações direta e inversa, são classificados como ácidos, respectivamente:
O pH dessa solução é
Dado log 3 = 0,5
Um composto que apresenta esse tipo de geometria é o
O mecanismo químico dessa reação é a
Ordenando-se as soluções em ordem crescente de pH, tem-se a seguinte sequência de solutos:
A porcentagem de rendimento dessa reação é igual a
Dado H = 1 g mol-1 , C = 12 g mol-1 , O = 16 g mol-1
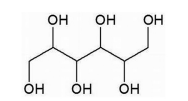
O número de átomos de carbono assimétrico no composto apresentado na fórmula estrutural é igual a
CaC2 O4 (s) → CaO (s) + CO (g) + CO2 (g)
Após o resfriamento, a massa de óxido de cálcio na amostra foi de 112 mg.
A concentração de íons cálcio, em g L-1 , na solução aquosa é
Dado Ca = 40 g mol-1 , C = 12 g mol-1 , O = 16 g mol-1
As configurações eletrônicas do átomo de níquel no estado fundamental e do íon Ni2+ correspondem, respectivamente, a
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
A análise de uma substância forneceu os seguintes resultados:
• composição centesimal: 60,0% de C, 26,7% de O e 13,3% de H
• massa molar: 60,0 g mol-1
• a reação da substância com KMnO4 em meio básico sob aquecimento, com posterior acidificação, acarretou a formação de um ácido carboxílico
Essa substância é nomeada por
Dado
C = 12 g mol-1 , O = 16 g mol-1 ,
H = 1 g mol-1
A quantidade mais próxima, em milimol, de cobre nessa alíquota de solução é igual a
8Al (s) + 3Fe3 O4(s) = 9Fe(s) + 4Al 2 O3(s) + CALOR
Considere 100,0 g de alumínio de soldagem com pureza de 81% e que a reação tem 75% de rendimento, por causa da troca de calor com o ambiente.
A quantidade de ferro, em gramas, formada nesse processo é, aproximadamente, de
A lei de velocidade dessa reação, nas condições mencionadas, é a
Dentre esses procedimentos, o único que NÃO se adapta a esses preceitos é a
Dado F = 96.500 C mol-1
Em termos comparativos, em relação às outras duas substâncias, a banda espectral de
Cl - (aq) + Ag+ (aq) → AgCl (s)
Após o ponto de equivalência, continuou-se adicionando 10,00 mL de excesso do agente titulante até que a concentração de íons em solução (ver equação a seguir) atingisse o equilíbrio.
AgCl (s) ⇄ Cl - (aq) + Ag+ (aq)
A concentração de Cl - na solução, em mol L-1 , será aproximadamente de
Nessa abordagem, no caso de uma titulação redox monitorada com um eletrodo combinado, graficamente obtém-se a(o)
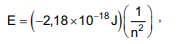
onde E é a energia da órbita permitida para um elétron no átomo de hidrogênio, em Joule, e n representa o número quântico principal que assume valores inteiros de 1, 2, 3, ... ∞ .
Dessa forma, com base nesse modelo atômico, para Bohr a(o)