Questões de Concurso Público UFPE 2019 para Químico
Foram encontradas 80 questões
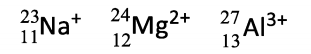
Sobre esses íons, analise as afirmações a seguir. 1) A ordem crescente de raio iônico é Al3+< Mg2+ < Na+. 2) São isoeletrônicos, pois possuem o mesmo número de elétrons. 3) Os cátions sódio e magnésio são isótonos.
Está(ão) correto(s):
Abaixo se encontra representada a tabela periódica com quatro elementos destacados, denominados D, R, X e K (esses não são os símbolos reais dos elementos).
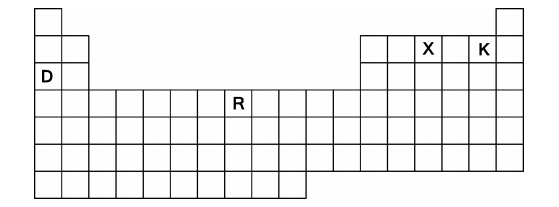
Sobre esses elementos, um estudante escreve: “Os elementos D, R, X e K são muito comuns na natureza. D possui
_______________acentuado e forma com K o composto________ DK. R é ___________ na temperatura ambiente e X
existe em_____________na atmosfera terrestre.” Os espaços em branco são corretamente preenchidos, na ordem, por:
O diagrama abaixo mostra os níveis de energia dos orbitais atômicos e moleculares envolvidos na formação de uma
espécie diatômica de oxigênio (Z = 8).
.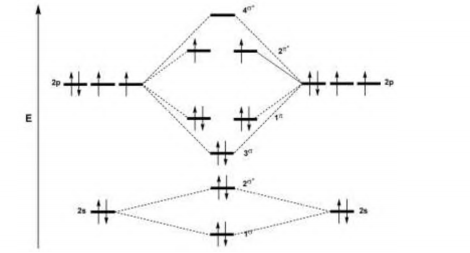
É correto afirmar que a espécie diatômica formada e a ordem de ligação (OL) são, respectivamente:
Um método clássico de se obter ferro é a partir da redução da hematita (Fe3Ü2), de acordo com a reação abaixo

Realizando o processo descrito acima e considerando uma siderúrgica com produção diária de 2,8 toneladas de ferro,
calcule o volume de dióxido de carbono liberado por dia, a 1 atm e 27ºC. Massas molares (g/mol): C = 12; O = 16; Fe = 56
Acerca da substância H2SO4, e considerando as condições ambientais 1 atm e 25 ºC, analise as afirmativas a seguir.
1) É um gás incolor e inodoro.
2) É solúvel em água.
3) Pode atuar como agente redutor.
É correto o que se afirma em apenas:
O hidrogênio é um elemento que forma compostos binários com vários outros elementos, metais e ametais, formando substâncias com propriedades químicas e físicas muito variadas. Em alguns casos, formam-se hidretos, que são compostos em que o hidrogênio é o elemento mais eletronegativo. Abaixo são mostrados alguns compostos binários de hidrogênio:

Entre os exemplos citados, há quantos hidretos?
A potenciometria se baseia na medida do potencial de células eletroquímicas, sem o consumo apreciável de corrente.
Aponte, entre os termos abaixo, o único que não está relacionado ao estudo dos métodos potenciométricos.
Em um laboratório de oceanografia química, um técnico analisou uma amostra de água de um canal e percebeu elevada turbidez. Acerca dessa característica, considere as afirmativas a seguir.
1) Deve-se à presença de íons em solução, como sódio e nitrato (Na+ e NO3").
2) É causada pela presença de partículas em suspensão que podem ter origem orgânica ou inorgânica.
3) Pode ser medida em laboratório utilizando-se um turbidímetro.
Está(ão) correta(s), apenas:
Um acidente ambiental provocou a contaminação das águas de um estuário com chumbo. Uma amostra de 200,0 mL foi coletada para análise e todo o chumbo foi precipitado na forma de PbSO4 devido ao tratamento da amostra com ácido sulfúrico. Sabendo que a massa obtida de PbSO4 foi 6,06 mg, qual é a concentração de chumbo na amostra, em mg/L?
Massas molares (g/mol): O = 16; S = 32; Pb = 207.
Um químico recebeu a tarefa de confirmar o conteúdo de um frasco não etiquetado no qual, supostamente, armazenou-se iodobenzeno. Para se certificar de que realmente se tratava de iodobenzeno, ele solicitou que fosse realizada uma análise de espectrometria de massas. O conteúdo do frasco será confirmado se o espectro obtido for:
Massas molares (g/mol): H = 1, C = 12 e I = 127.
Na padronização de uma solução de Ba(OH)2, utilizou-se 0,61 g do padrão primário ácido benzoico (C6H5COOH). O ponto final foi observado após a adição de 250,0 mL da solução básica. É correto afirmar que a concentração molar de Ba(OH)2 na solução é:
Massas molares (g/mol): H = 1, C = 12, O = 16 e Ba = 137.
Um estudante se esqueceu de anotar no caderno qual foi o solvente utilizado em uma reação. Ao conversar com seu professor, ele explicou que estava na dúvida entre hexano, acetato de etila, etanol, éter dietílico e tolueno, que eram os solventes disponíveis no laboratório no dia do experimento. Ele relatou também que tinha separado uma pequena amostra do solvente. O professor respondeu que seria fácil tirar a dúvida e levou a amostra para uma análise de espectroscopia de infravermelho, chegando ao seguinte espectro:
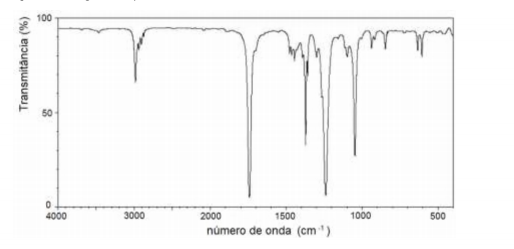
A partir do espectro obtido, pode-se afirmar que o solvente utilizado pelo estudante foi
A decomposição do oxalato de cálcio hidratado foi estudada utilizando-se análise termo gravimétrica em recipiente aberto. Sabe-se que, com o aquecimento, sucessivas decomposições ocorrem, de acordo com as equações abaixo:
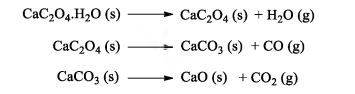
A curva de decomposição térmica esperada para esta análise é:
Para determinar a pureza de uma amostra de 500,0 mg de Na2B4O7(s), um técnico realizou uma titulação com solução de HCl 0,020 M. A reação é:
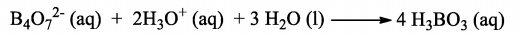
Sabendo que o volume utilizado da solução ácida foi 200,0 mL, é correto afirmar que a pureza da amostra em termos percentuais é:
Massas molares (g/mol): H = 1; B = 11; O = 16; Na = 23; Cl = 35,5.