Questões de Concurso Público IF-RS 2018 para Técnico de Laboratório - Química
Foram encontradas 40 questões
A seguir são apresentadas as fórmulas estruturais do Aspartame e do Neotame:
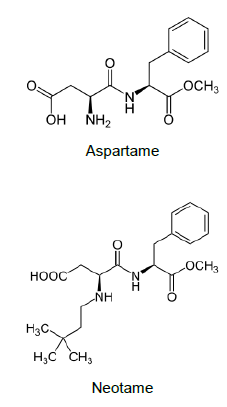
A alternativa que contém a função orgânica que NÃO está presente na estrutura do Aspartame e do Neotame é
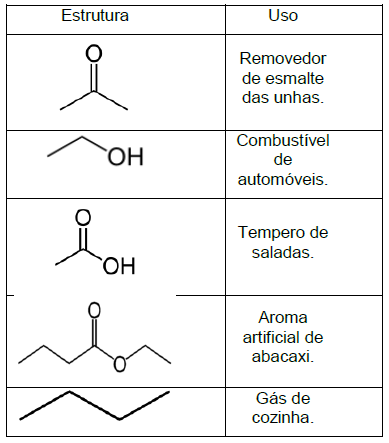
A sequência CORRETA que apresenta o nome dos compostos orgânicos, de cima para baixo, é:
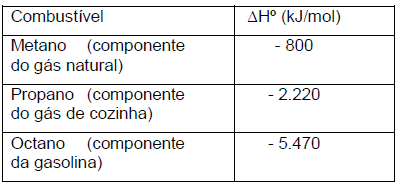
Com base nesses dados, são feitas as seguintes afirmativas:
I. O poder calorífico do Propano é maior que do Octano. II. A queima de um mol de Metano absorve cerca de 50 kJ de energia. III. A energia proveniente da queima de 1 kg de Metano é cerca de 2,8 vezes menor que a energia da queima de 1 kg de Propano.
Assinale a alternativa em que toda(s) a(s) afirmativa(s) está(ão) CORRETA(S):
N2O5(g) + H2O(l) → 2 HNO3(aq)
Utilizando as equações termoquímicas:
N2(g) + 3 O2(g) + H2(g) → 2 HNO3(aq) ∆H= – 415 kJ 2 H2(g) + O2(g) → 2 H2O (l) ∆H= – 572 kJ 2 N2(g) + 5 O2(g) → 2 N2O5(g) ∆H = + 22 kJ
Assinale a alternativa que contém o valor da entalpia envolvida na obtenção de quatro mols de ácido nítrico:
“Normal”: 60 g de sacarose em frascos de 500 mL. “Light” (teor reduzido de açúcar): 100 g de sacarose em frascos de 1 L. Dado: densidade do refrigerante a 20 °C = 1,04 g/mL
Assinale a alternativa em que a afirmativa está INCORRETA: