Questões de Concurso Público UFPR 2017 para Técnico de Laboratório - Química
Foram encontradas 20 questões
A calda bordalesa, muito utilizada como fungicida na agricultura, é preparada pela mistura de sulfato de cobre pentaidratado (CuSO4.5H2O), um pequeno excesso de cal (CaO) e água em proporção de 1:1:10 (m:m:v), respectivamente, obtendo-se uma suspensão muito fina (partículas pequenas).
De acordo com os dados de constante de solubilidade, assinale a alternativa que apresenta o constituinte principal do sólido suspenso na calda bordalesa.
Foi realizada uma aula experimental visando a síntese de uma amida aromática, a acetanilida (ou N-fenil-acetamida), de acordo com o procedimento experimental resumidamente descrito a seguir:
Em um béquer limpo e seco, misturar o ácido acético glacial e o acetato de sódio anidro. Adicionar a anilina e, em seguida, o anidrido acético. Após 10 minutos de reação, verter o meio reacional sobre água destilada gelada, sob agitação. A acetanilida precipita. Filtrar em funil de Büchner e lavar o produto bruto com água destilada gelada até pH neutro. Purificar a acetanilida por recristalização usando água quente e carvão ativado.
Sobre esse procedimento, considere as seguintes afirmativas:
1. A reação envolvida na síntese da acetanilida é uma reação de acilação.
2. Foi utilizada água gelada na etapa de precipitação da acetanilida bruta para reduzir as perdas de produto por solubilidade em água.
3. A purificação do produto bruto foi realizada em água quente porque a acetanilida é mais solúvel em água quente que em água fria.
4. O carvão ativado foi utilizado para acelerar a precipitação da acetanilida.
Assinale a alternativa correta.
O ácido nítrico “branco” (100% puro; P.E. = 83 ºC) pode ser obtido em laboratório por destilação de uma mistura de KNO3 e H2SO4, como mostra a reação a seguir:
KNO3 + H2SO4 → HNO3 + KHSO4
Tendo em vista que o HNO3 é decomposto por aquecimento a NO2 e H2O, assinale a alternativa que apresenta a técnica de
destilação que deve ser utilizada nesse processo.
Sabões são sais de sódio ou potássio de ácidos graxos, obtidos pela reação de gorduras e óleos (triglicerídeos) com NaOH, KOH ou Na2CO3. A reação de saponificação é representada a seguir:
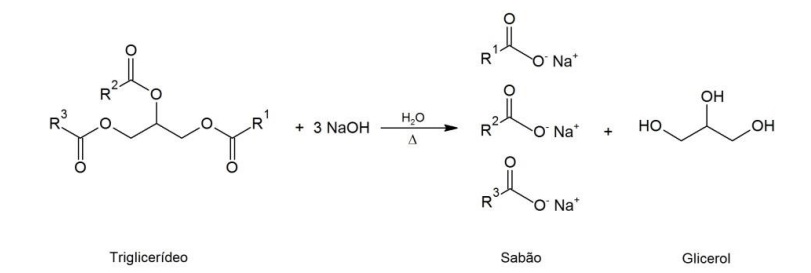
em que R1 , R2 e R3 são cadeias lineares saturadas ou insaturadas, geralmente com doze ou mais átomos de carbono.
Com base nessas informações, considere as seguintes afirmativas:
1. Uma solução aquosa de sabão puro apresenta pH < 7.
2. Adição de ácido forte a uma solução de sabão acarreta precipitação de ácidos graxos.
3. Ca(OH)2 não pode ser usado na obtenção de sabão, pois sais de cálcio de ácidos graxos são insolúveis em água.
4. A obtenção de sabão com Na2CO3 segue a mesma estequiometria que no uso do NaOH.
Assinale a alternativa correta.
As atividades realizadas nos laboratórios didáticos de Química precisam ser acompanhadas do descarte correto dos resíduos produzidos durante as aulas experimentais, sendo importante classificar os resíduos e escolher o tratamento mais adequado. Nesse sentido, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
1. Resíduos básicos concentrados, p. ex. aminas. / ( ) Tratar com sulfito de sódio e depois ajustar o pH entre 7 e 9.
2. Resíduos fortemente oxidantes em solução, p. ex. permanganato. / ( ) Recobrir o resíduo com enxofre em pó e armazenar.
3. Resíduo de mercúrio metálico. / ( ) Diluir até obtenção de uma solução com pelo menos 50% de água (em volume) e, em seguida, ajustar o pH entre 7 e 9.
4. Resíduo contendo sais de cianeto em solução aquosa diluída. / ( ) Adicionar 1 grama de NaOH por 100 mL de solução. Adicionar água sanitária.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.