Questões de Concurso Público UFC 2017 para Médico - Pesquisa Clínica
Foram encontradas 50 questões
De acordo com a Resolução da Diretoria Colegiada da Anvisa de 2015 que dispõe sobre o Regulamento para a realização de ensaios clínicos com medicamentos, um evento adverso grave é aquele que resulte em qualquer experiência adversa com medicamentos, produtos biológicos ou dispositivos, ocorrendo em qualquer dose e que resulte em qualquer um dos seguintes desfechos:
I. Ameaça à vida e/ou óbito.
II. Incapacidade/invalidez persistente ou significativa.
III. Exige internação hospitalar ou prolonga internação.
IV. Anomalia congênita ou defeito de nascimento.
V. Evento clinicamente significante.
VI. Qualquer suspeita de transmissão de agente infeccioso por meio de um medicamento.
O correto está em:
De acordo com a Resolução da Diretoria Colegiada da Anvisa de 2015 que dispõe sobre o Regulamento para a realização de ensaios clínicos com medicamentos, o Investigador:
I. Deve supervisionar pessoalmente o ensaio clínico, podendo delegar tarefas e responsabilidades.
II. Deve conduzir o ensaio clínico de acordo com o protocolo acordado com patrocinador, com as boas práticas clínicas, com as exigências regulatórias e éticas aplicáveis e vigentes.
III. Deve assegurar a assistência médica adequada aos participantes do ensaio clínico quanto a quaisquer eventos adversos relativos ao ensaio clínico, incluindo valores laboratoriais clinicamente significativos, sem qualquer ônus para o participante.
IV. É responsável por armazenar os produtos sob investigação conforme especificação do patrocinador e em consonância com as exigências regulatórias aplicáveis.
V. Deve informar prontamente os participantes do ensaio clínico quando este for finalizado prematuramente ou suspenso por qualquer motivo, além de assegurar terapia apropriada e acompanhamento aos participantes.
O correto está em:
Segundo a Resolução Nº 466 de 12/12/2012, do Conselho Nacional de Saúde, o protocolo de pesquisa completo, a folha de rosto e demais documentos dos seguintes tipos de estudos clínicos devem ser encaminhados para apreciação pela CONEP (Comissão Nacional de Ética em Pesquisa):
I. Pesquisas com cooperação estrangeira.
II. Envio para o exterior de material genético ou qualquer material biológico humano para obtenção de material genético, salvo nos casos em que houver cooperação com o governo brasileiro.
III. Estudos em crianças.
IV. Estudos que envolvem equipamentos e dispositivos terapêuticos, novos ou não registrados no País.
O correto está em:
Os princípios éticos baseados primariamente na Declaração de Helsinki devem ser a base para a aprovação e condução dos ensaios clínicos. Três princípios éticos básicos de igual força moral, a saber, respeito pelas pessoas, beneficência e justiça, permeiam todos os princípios de BPC. Baseado nesses princípios éticos, analise as afirmativas abaixo e marque a alternativa correta.
I. Os ensaios clínicos devem ser conduzidos apenas se os benefícios antecipados para o indivíduo sujeito da pesquisa ultrapassarem claramente os riscos envolvidos. Entretanto, se os benefícios dos resultados do ensaio clínico forem importantes para a ciência e a sociedade justifica-se o uso do sujeito da pesquisa mesmo que o referido ensaio clínico possa colocar em risco a sua segurança e bem-estar.
II. Um ensaio clínico deve ser sempre conduzido em consonância com o protocolo que recebeu aprovação/opinião favorável anteriormente por parte da comissão de revisão institucional (CRI)/comitê independente de ética (CEI).
III. Deve-se obter o consentimento informado dado livremente por cada sujeito antes da participação nos ensaios clínicos. Entretanto, se o sujeito da pesquisa for analfabeto ele está dispensado do consentimento informado.
IV. Somente os médicos podem conduzir ensaios clínicos com pacientes. Esses profissionais devem ser qualificados adequadamente por meio de educação, treinamento e experiência para desempenhar suas tarefas relativas ao ensaio clínico e aos sujeitos da pesquisa.
V. A privacidade dos registros que poderiam identificar os sujeitos deve ser protegida, respeitando a privacidade, e as regras de privacidade.
O correto está em:
Segundo a Resolução Nº 466 de 12/12/2012 do Conselho Nacional de Saúde, em se tratando do Termo de Consentimento Livre e Esclarecido – TCLE:
I. Deverá ser adaptado, pelo pesquisador responsável, nas pesquisas com cooperação estrangeira concebidas em âmbito internacional, às normas éticas e à cultura local.
II. São elementos do TCLE: a anuência do participante da pesquisa e/ou de seu representante legal; os tratamentos envolvidos no estudo, e explicitação da garantia de ressarcimento.
III. Nos casos em que seja inviável a obtenção do TCLE, a dispensa do TCLE deve ser justificadamente solicitada pelo pesquisador responsável ao Sistema CEP/CONEP, para apreciação, sem prejuízo do posterior processo de esclarecimento.
IV. No TCLE podemos omitir informações desde que a pesquisa dependa de restrição de informações aos seus participantes.
O correto está em:
Qual o fluxo regulatório para um projeto de pesquisa denominado “estudo multicêntrico nacional, Fase III em pacientes com câncer gástrico”, em que você é um dos investigadores.
O correto está em:
O dossiê de desenvolvimento clínico de medicamento (DDCM) submetido à Anvisa deve ser composto de várias informações e documentos, entre eles:
I. Brochura do Investigador contendo as informações de segurança e eficácia em humanos obtidos a partir de ensaios clínicos já realizados; e possíveis riscos e eventos adversos relacionados ao medicamento experimental, baseados em experiências anteriores, bem como precauções ou acompanhamentos especiais a serem seguidos durante o desenvolvimento.
II. Comprovante de registro do ensaio clínico em base de dados de registro da International Clinical Trials Registration Platform / World Health Organization ou outras reconhecidas pelo International Committee of Medical Journals Editors.
III. Descrição do medicamento experimental, incluindo: os resultados de estudos de estabilidade que assegurem a utilização do medicamento experimental nos ensaios clínicos planejados.
IV. Descrição geral do processo de fabricação e embalagem com informações sobre a capacidade dos equipamentos.
V. Plano de desenvolvimento do medicamento informando a fase, desenho, desfechos, comparadores, objetivos, população a ser estudada, hipótese(s), número estimado de participantes e planejamento estatístico para cada ensaio clínico planejado.
O correto está em:
A pesquisa e o desenvolvimento de novos medicamentos envolvem atividades multiprofissionais que culminam com a pesquisa com seres humanos. Esses estudos estão divididos em Fases I, II, III e IV. Nesse sentido, em que fase ou fases são avaliadas a segurança e a dosagem dos medicamentos?
O correto está em:
Estima-se que em torno de 40% dos medicamentos fracassem nos estudos Fase I. Baseado nessas observações, preconizou-se a realização de estudos Fase 0. Analise as afirmações abaixo.
I. Utiliza-se uma dose única bem abaixo da HED (human equivalente dose/dose equivalente em humano) do fármaco em estudo.
II. Permite a determinação da segurança do fármaco em estudo.
III. Fornece informações iniciais sobre a farmacocinética do fármaco em estudo.
O correto está em:
Os estudos Fase II são algumas vezes divididos em IIA e IIB. Analise as afirmações abaixo.
I. No Fase IIA estuda-se a eficácia com um pequeno número de pacientes e habitualmente uma única dose.
II. No Fase IIB o estudo é conduzido com maior número de pacientes e é planejado para determinar as doses que serão utilizadas no estudo Fase III.
III. No Fase IIA não se estuda a farmacocinética do fármaco.
O correto está em:
Os estudos Fase IV são realizados após a aprovação e comercialização dos medicamentos. Analise as afirmações abaixo e marque a alternativa correta.
I. Comparar com outros medicamentos visando ampliar a experiência de uso.
II. Identificar e relatar reações adversas.
III. Avaliar o risco e o benefício do uso a longo prazo.
O correto está em:
Os ensaios clínicos são enquadrados em diferentes fases. Julgue as afirmações subsequentes e marque a alternativa correta.
I. Os estudos da Fase I visam estabelecer o espectro de ação clínica, ou resposta, de uma substância ou combinação de fármacos.
II. Estudos da Fase II são desenhados para se definir a relação entre a dose e a toxicidade de determinado medicamento. Eles servem, ainda, para testar modos diferentes de administração de um mesmo tratamento.
III. Os estudos da Fase III são realizados para se confirmar que os resultados obtidos na fase anterior são aplicáveis em uma grande parte da população doente. Nessa fase, o medicamento já foi aprovado para ser comercializado.
IV. Nos estudos da Fase IV, são exploradas novas indicações de determinado fármaco, além de avaliados os possíveis efeitos colaterais em grandes populações (farmacovigilância).
V. A farmacovigilância também é responsável pela elaboração de projeções sobre o impacto econômico da incorporação de medicamentos no tratamento de determinadas doenças.
O correto está em:
A pesquisa clínica pode ser conduzida através de diversos tipos de ensaios clínicos. Analise as afirmativas abaixo e marque a alternativa correta.
I. No Estudo aberto comparativo o medicamento estudado será comparado com fármaco análogo ou placebo, porém médico e paciente não terão conhecimento de quem está em qual grupo.
II. No estudo cruzado os sujeitos da pesquisa servem como seus próprios controles.
III. No Estudo paralelo os diferentes tratamentos são ministrados ao mesmo grupo de pacientes, que são comparáveis entre si, durante todo o tempo planejado de estudo.
O correto está em:
Os procedimentos analíticos de um ensaio clínico vão depender da natureza do estudo, dos parâmetros estimados, e dos efeitos que foram medidos. O plano de análise do ensaio clínico deve estar incluído no protocolo. Nesse contexto, julgue os itens a seguir.
I. Em estudos do tipo caso-controle, quando se quer comparar dois grupos mediante de suas respostas em uma variável dicotômica por meio de um aplicativo estatístico, usa-se o teste t de Student.
II. O teste qui-quadrado, serve para verificar se a frequência com que determinado acontecimento observado em uma amostra se desvia significativamente ou não da frequência com que ele é esperado.
III. O risco relativo calculado em um aplicativo estatístico representa uma relação (ratio) da probabilidade de o evento ocorrer no grupo exposto contra o grupo de controle (não exposto), sendo muito utilizado em estudos de caso-controle.
IV. Uma análise de dados mais rigorosa é chamada de intenção de tratamento e inclui todos os indivíduos que iniciaram o ensaio clínico, independente se eles concluíram a intervenção e período de seguimento. Considera-se como falha terapêutica todos os casos que foram retirados do estudo por razões de efeitos colaterais e aqueles nos quais não foi possível completar o seguimento de avaliação.
O correto está em:
Sabendo-se que os ensaios clínicos aleatorizados são investigações científicas consideradas padrão de excelência em estudos científicos que pretendem avaliar o efeito de um tratamento medicamentoso no curso de uma doença, analise as afirmativas abaixo e marque a alternativa correta.
I. Trata-se de um estudo experimental, onde se isola a contribuição singular de um fator mantendo-se constante, sempre que possível, os outros determinantes do desfecho.
II. Elege-se o tipo de população alvo da intervenção, estabelecendo-se os critérios de elegibilidade (inclusão e exclusão).
III. A alocação aleatória permite a geração de grupos verdadeiramente comparáveis, de modo que cada paciente tem a mesma probabilidade de pertencer a um dos grupos (exposto ou não-exposto), desde que todos preencham os critérios de elegibilidade.
IV. Todos os fatores relacionados ao prognóstico e ao desfecho tendem a ser igualmente distribuídos nos grupos de comparação. Desse modo, eventuais diferenças na ocorrência do desfecho entre os grupos experimental e controle podem ser atribuídas à intervenção.
V. Para a aleatorização ser válida é necessário que cada paciente elegível tenha chance igual de ser alocado para cada um dos grupos do estudo e não pode haver influências dos investigadores.
O correto está em:
Um pesquisador deseja dimensionar a amostra de um ensaio clínico, tomando como base o desfecho primário, que constitui uma variável contínua. Para tanto, ele necessita atribuir valores para os parâmetros utilizados no cálculo, quais sejam: a probabilidade máxima do erro tipo I (nível de significância, α), a probabilidade máxima do erro tipo II (β) e poder estatístico (1 – β), a diferença a ser detectada (magnitude do efeito, δ) e a variabilidade da variável de desfecho (desvio padrão, σ).
Analise as seguintes sentenças acerca da influência de tais parâmetros no tamanho da amostra, e marque a alternativa correta.
I. Quanto maior α, maior o tamanho da amostra.
II. Quanto maior o poder (1 – β), maior o tamanho da amostra.
III. Quanto maior σ, maior o tamanho da amostra.
IV. Quanto maior δ, maior o tamanho da amostra.
V. Quanto maior a razão δ/σ, menor o tamanho da amostra.
O correto está em:
Durante o planejamento do tamanho da amostra de um ensaio clínico, o pesquisador, rotineiramente, atribui para a probabilidade máxima do erro tipo I (α = 5%) um valor menor que o estabelecido para a probabilidade máxima do erro tipo II (β = 20%).
Analise as proposições acerca das razões para tal procedimento e, em seguida, assinale a alternativa correta.
I. É menos grave o risco de atribuir equivocadamente eficácia a um determinado fármaco do que concluir erroneamente que um dado fármaco é ineficaz.
II. O risco de atribuir equivocadamente eficácia a um determinado fármaco é mais grave do que concluir erroneamente que um dado fármaco é ineficaz.
III. Concluir erroneamente que um dado fármaco é ineficaz é tão grave quanto atribuir equivocadamente eficácia a um determinado fármaco.
IV. Um resultado falso-positivo acerca da eficácia de um fármaco é mais prejudicial do que um resultado falso-negativo;
V. Um resultado falso-positivo acerca da eficácia de um fármaco é menos prejudicial do que um resultado falso-negativo.
O correto está em:
A figura abaixo ilustra o gráfico da pressão arterial sistólica (PAS) em função do tempo. Os pontos correspondem aos valores médios da PAS de pacientes hipertensos tratados com dois fármacos antihipertensivos ao longo de 90 dias (D90). No dia zero (D0), efetuou-se a medida basal (pré-tratamento) da PAS.
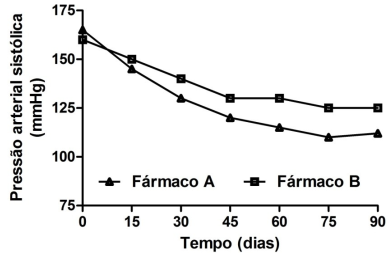
Assinale, dentre os parâmetros abaixo, aquele que avalia, de forma mais apropriada, o efeito anti-hipertensivo
global.