Questões de Concurso Público UFES 2015 para Técnico de Laboratório - Química
Foram encontradas 28 questões
Cr2O72-(aq) + 6Fe2+(aq) + 14H+(aq) -› 2Cr3+(aq) + 6Fe3+(aq) + 7H2O(l)
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é, aproximadamente, igual a

Com base nos dados tabelados, são considerados “eletrodos de sacrifício” adequados as barras de
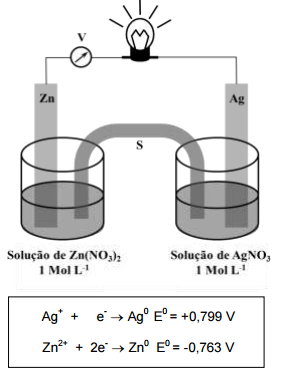
Considerando a célula eletroquímica e os potenciais-padrão de redução acima representados, é CORRETO afirmar:
SO2(g) + ½O2(g) ⇋ SO3(g)
A expressão da constante de equilíbrio KC, com base na lei de ação das massas, para esta reação é