Avalie as duas reações de combustão a seguir e escolha a al...
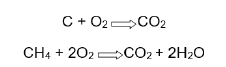
Comentários
Veja os comentários dos nossos alunos
Combustão do Carbono
A combustão do carbono é dada por:
C + O2 ==> CO2
Esta equação significa que 1 kmol de carbono ao reagir com 1 kmol de oxigênio forma1 kmol de dióxido de carbono liberando energia. Ela também significa que 12 kg de carbono reagem com 32 kg de oxigênio para gerar 44 kg de dióxido de carbono liberando, de acordo com a questão, 9,09 kWh/kg de energia térmica. Do ponto de vista ambiental, esta reação gera 3,66 kg de dióxido de carbono por kg de carbono ou 0,403 kgCO2/kWh.
Combustão do Metano
O Metano é o hidrocarboneto mais simples e, quando se queima um hidrocarboneto, tanto o carbono como o hidrogênio são oxidados e se transformam em dióxido de carbono e água. No caso do Metano, a combustão seguirá a seguinte equação:
CH4 + 2O2 ==> CO2 + 2H20
Neste caso, 16,04 kg de metano geram 44 kg de dióxido de carbono. Ou seja, apenas 2,74 kg de dióxido de carbono são gerados por kg de metano. Isto representa 25% menos dióxido de carbono por quilo de combustível se comparado com o carbono.
Do ponto de vista energético, os 16,04 kg de Metano geram, conforme a questão, 14 kWh/kg por kg de combustível, que representa 0,20 kgCO2/kWh. Isto significa que o Metano gera cerca da metade do CO2 gerado pela combustão do carbono. É importante observar que este número não leva em consideração a eficiência das máquinas térmicas.
---
Gabarito: B
Oi, vim aqui pra deixar uma dica de um site para estudo de química com foco em concursos públicos. Baixe resumos de química grátis no site: http://quimicaparaconcursos.com e bons estudos!
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo