Pelo modelo de repulsão de pares de eletrônicos da camada d...
- Gabarito Comentado (1)
- Aulas (2)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
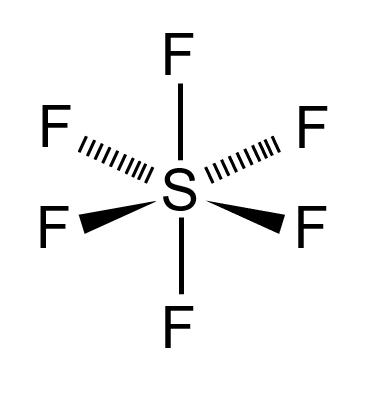
B) CORRETA - Conforme mostrado na imagem acima, a geometria da molécula do SF6 é octaédrica, pois são 7 átomos, sendo que o enxofre é o átomo central (sem a presença de elétrons não ligantes) ligado a outros 6 átomos de flúor.
C) INCORRETA - Na geometria bipiramidal são necessários 6 átomos, cujo átomo central, que não apresenta elétrons não ligantes, se liga a outros 5 átomos.
D) INCORRETA - Nessa geometria são necessários 5 átomos, com o átomo central ligado a outros 4 átomos, que estão localizados no mesmo plano (há a presença de elétrons livres no átomo central).
E) INCORRETA - Nessa geometria são necessários 6 átomos, cujo átomo central está ligado a 4 átomos em um mesmo plano e a outro átomo em um plano diferente, formando uma pirâmide quadrangular (há a presença de elétrons livres no átomo central).
Gabarito do Professor: Letra B.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
SF6: 6 ligantes, nenhum par de elétrons livres = sistema octaédrico
Moléculas com 6 ligantes que não possuem pares de elétrons isolados (não-ligantes) no átomo central possuem geometria octaédrica, caso do SF6. Gabarito: B
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo