A reação de equilíbrio a seguir ocorre à pressão de 1 bar, ...
NH3(g) ⇔
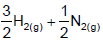
O valor correspondente de Kc (T) para essa reação no estado padrão de 1 mol L-1 é de
Dado Constante dos gases, R=0,083145 L.bar.mol-1 .K-1
Comentários
Veja os comentários dos nossos alunos
somente aplicar a fórmula de conversão de Kc=Kp(RT)^(mol reagente-mols produto)
Kc= 1,36.10^-3 ( 0,0083145.298)^-1
Kc= 5,5.10^-5
A fórmula correta seria:
Kp=Kc(RT)^(mol reagente-mols produto)
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo