Uma amostra (100,0 mL) de água foi coletada e seu pH inicial...
Dados: massa molar CaCO3 = 100,0 g mol-1 .
Comentários
Veja os comentários dos nossos alunos
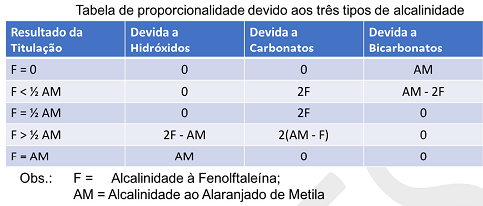
Na tabela carbonato: F>1/2AM
calcula-se:
2(14,5-9,8) *0,01M * 100000/ 100mL = 94
pH de viragem da fenolftaleína, F = 8,3
pH de viragem do alaranjado de metila, AM = 4,5
F > 1/2 AM
Na tabela carbonato:
CaCO3 = 2 * ( AM - F )
CaCO3 = 2 * ( 14,5 mL - 9,8 mL ) * ( 1L / 1000 mL ) * ( 0,01 mol / L )
CaCO3 = 9,4*10^-5 mol CaCO3
Calculando a concentração de CaCO3 (mg/L):
( 9,4*10^-5 mol CaCO3 / 100 mL ) * ( 1000 mL / 1L ) * (100 g / 1 mol CaCO ) * (1000 mg / 1 g )
= 94 g CaCO3
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo