Os estudos em mecânica quântica possibilitaram a organização...
Os estudos em mecânica quântica possibilitaram a organização dos elétrons em orbitais, permitindo conhecer a configuração eletrônica de cada elemento químico representado na tabela periódica. Uma das aplicações dessa configuração é conhecer o número de elétrons na camada de valência, e, com isso, prever o número de elétrons envolvidos e/ou o tipo de ligação química que esse elemento tende a fazer.
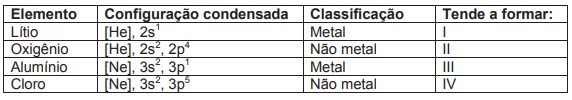
Dessa forma, considerando os elementos abaixo, assinale a alternativa que apresente, em I, II, III e IV, os íons que cada elemento tende a formar.