Considerando-se o Texto 1, qual é o valor da constante k da ...
Comentários
Veja os comentários dos nossos alunos
Para começar, vamos determinar as O.R de cada reagente:
Logo de cara nos deparamos com um obstáculo, nenhuma [C] permanece constante, então vamos começar por ele:
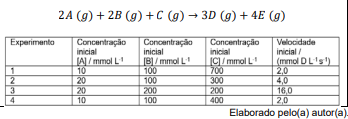
Se pegarmos os experimentos 1 e 4, temos que as [A] e [B] permanecem constantes, apenas a [C] varia, portanto, apenas essa alteração irá contribuir. Porém, apesar da [C] variar, a velocidade não muda. Portanto a O.R de C = 0, ou seja, ele não interfere na velocidade de reação. Com isso, podemos seguir para as demais concentrações:
O.R [A] = experimento 1 e 2.
As [A] aumentam 2x e a v também aumenta 2x, portanto teremos a O.R = 2^x = 2
x = 1
Portanto, O.R [A] = 1
O.R [B] = experimento 2 e 3.
As [A] permanecem constantes e a [B] aumenta em 2x. A v aumenta em 4x, portanto temos:
O.R = 2^y = 4
y = 2, portanto O.R [B] = 2
Agora que definimos todas as ordens de reação, substituímos na fórmula da lei da velocidade:
v = k * [A]^x * [B]^y * [C]^z
=> v = k * [A]^1 * [B]^2 * [C]^0
*** Todo número elevado a 0 resulta em 1
*** Todo número elevado a 1 é igual a ele mesmo
=> v = k * [A] * [B]^2 * 1
Agora substituímos os valores de qualquer um dos experimentos da tabela nesta fórmula e encontramos o valor de k
=> Exp. 4
=> 2 = k* 10 * 100^2
=> 2 = k 10 * 10.000
=> 2 = k * 100.000
=> 2 / 100.000 = k
Portanto, k = 2.10^-5
Rever
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo