O jeans com aspecto “desbotado” pode ser obtido pela oxidaçã...
O jeans com aspecto “desbotado” pode ser obtido pela oxidação parcial do índigo impregnado no tecido (denim), utilizando-se uma solução de KMnO4, como ilustrado pelo esquema reacional a seguir. Devido à formação de MnO2, sólido castanho insolúvel em água, um outro reagente deve ser usado para que ele não impregne o tecido.
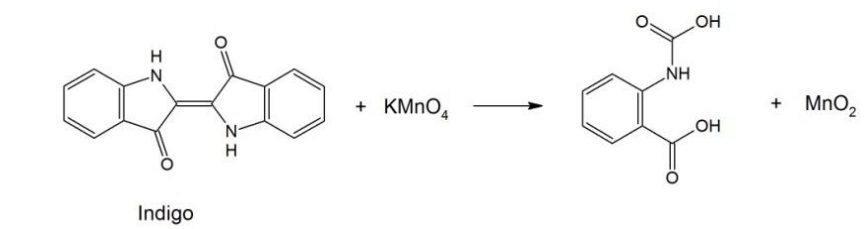
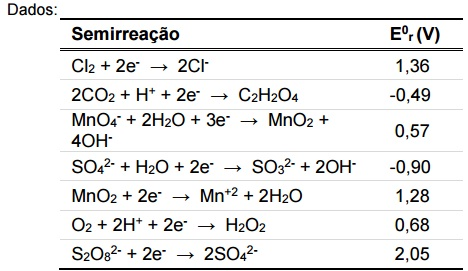
De acordo com os potenciais de redução fornecidos na tabela
ao lado, assinale a alternativa que apresenta substâncias que
podem ser usadas para transformar o MnO2 na espécie
solúvel Mn+2
.
Comentários
Veja os comentários dos nossos alunos
As substâncias para reagir precisam ser adicionadas no meio em sua forma reduzida para então sofrerem oxidação e reduzir o MnO2
Quanto maior for o potencial de redução de uma reação, maior é sua tendência se reduzir. A reação que a questão quer que ocorra é a transformação do MnO₂ (em que o Mn tem nox +4) em Mn⁺², que é uma reação de redução com potencial de 1,28V, como indicado na tabela. Assim, as substâncias usadas para efetivar essa reação, devem se oxidar, o que só acontece se o potencial de redução da reação em que estão envolvidas for menor que 1,28V. Como as reações da tabela são de redução e as que devem ocorrer são de oxidação, é importante lembrar de pensar na reação de forma invertida (com os reagentes como produtos e os produtos como reagentes).
Assim, tem-se que as únicas duas subtâncias das alternativas que se apresentam na tabela nos produtos e que estão envolvidas em reações com potencial de redução menor que 1,28V são H₂O₂ e C₂H₂O₄.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo