A dissolução de minerais presentes em solos e rochas ou, ain...
Observe a tabela a seguir.
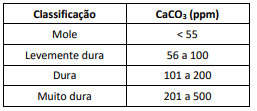
A análise de 120,0g de uma amostra de água de um manancial indicou a presença de 15,0mg de CaCO3. Essa amostra deve classificada como
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
fiz assim, pois nao lembrava da fórmula:
-transformei 120g em mg: 120.000mg = 1,2x10^5
-fiz isso dividido por 15mg
1,2x10^5 / 1,5x10^1 = 0,000125
-ai contei as casas da virgula e deu 6.
então cheguei em 125 ppm.
1 ppm = 1/1000000 =0,000001
mg=0,001g
mg =0,000001Kg
Divide
15 mg / 0,120 kg = 125ppm
ÁGUA DURA
LETRA C
Converte a massa da amostra de água para miligramas (mg):
120,0 g x 1000 = 120.000 mg
Calcula a concentração de CaCO₃ em ppm:
[ ] = (mCaCO₃/ mÁgua) × 10⁶
[ ] = (15,0 mg / 120.000 mg) × 10⁶
[ ] = 0,000125 × 10⁶
[ ] = 125 ppm
Alternativa C, dura.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo