Considere as três afirmativas a seguir sobre o ciclo aprese...
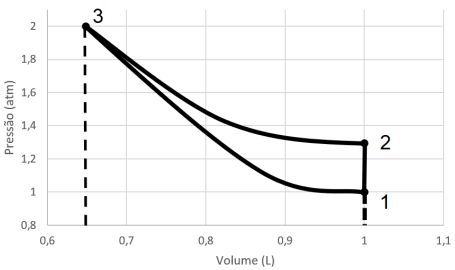
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale
- Gabarito Comentado (1)
- Aulas (4)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
I. A variação de entropia (ΔS) ao longo do ciclo é nula.
Variação de entropia (função de estado):
ΔS = Entropia(final) - Entropia(inicial)
Entropia(final) = Entropia(inicial)
ΔS = Entropia(final) - Entropia(inicial) = 0
II. A variação de trabalho (Δw) ao longo do ciclo é nula.
Aquecimento isovolumétrico (1 → 2) = Compressão adiabática: ΔU = w(1) (w(1) = p*Δv(1)), q = 0
Expansão adiabática (3 → 1): ΔU = -w(2) (w(2) = p*Δv(2))
Δw = w(2) – w(1), w(1) ≠ w(2)
Δw ≠ 0
III. A variação de energia interna ao longo do ciclo é nula.
Variação de energia interna (função de estado): ΔU = U - U
U(final) (1) = U(inicial) (1)
ΔU = U(final) - U(inicial) = 0
Entropia e Energia Interna são funções de estado.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo