O teor de grupos funcionais básicos em um carbono ativado fo...
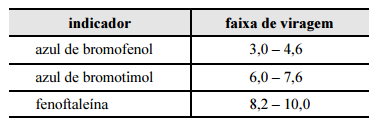
Considerando a situação descrita e a tabela apresentada, que contém faixas de viragem de diferentes indicadores, julgue o item subsequente. Em unidades de massa por volume, a concentração da solução de HCl 0,100 mol/L é superior à da solução padrão de NaOH 0,100 mol/L.
- Gabarito Comentado (1)
- Aulas (11)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
MMHCl = 1,0 + 35,5 = 36,5 g/mol
MMNaOH = 23,0 + 16,0 + 1,0 = 40 g/mol
Assim, é possível obter a concentração (C) multiplicando a molaridade (M) pela massa molar:
C = M ∙ MM
Logo:
CNaOH = 0,1 ∙ 40,0 = 4,00 g/L
Gabarito do Professor: ERRADO.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
A massa molar do NaOH é maior.
C(g/L) = M(mol/L) x MM(g/mol) --> C(HCl) = 0,1 x 36,5 ==> C(HCl) = 3,65g/L
C(NaOH) = 0,1 x 40 ==> C(NaOH) = 4,0g/L
C(NaOH) > C(HCl)
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo