Questões de Concurso
Comentadas para cesgranrio
Foram encontradas 24.821 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Tal opção significa que essa universidade priorizou uma estratégia de controle organizacional com
Dentre os diversos modelos contemporâneos sobre motivação, o que mais ajuda a explicar a percepção desses servidores é a teoria da(o)
Essa situação ilustra uma possível condição que estimula um conflito, denominada
Sendo assim, constata-se que essa universidade optou por uma estrutura organizacional denominada
Em uma universidade, optou-se pelo modelo de sistemas abertos, que favorece a
Pode-se caracterizar essa decisão como
Na Figura, representa-se um setor circular cujo ângulo central é α.
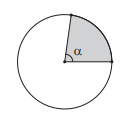
A área desse setor circular corresponderá a 2/3 da área do círculo quando α medir
Qual é a probabilidade de, escolhidos três processos ao acaso no mutirão, todos serem indeferidos?
Uma das funções de um processador é
O componente do Windows cuja função é impedir que malwares alcancem o computador, bloqueando arquivos suspeitos, é a(o)
Desse modo, as memórias são classificadas, desde seu alto custo e alta velocidade até sua maior capacidade de armazenamento, na seguinte ordem:
Com relação aos dispositivos de E/S, um dispositivo que serve para armazenamento externo de dados é a(o)
Para permitir essa implementação, deve ser adquirido o seguinte aparelho:
O número de DPI de um scanner representa a quantidade de
O serviço de filtragem e o sistema de interface das distribuições Linux Ubuntu 18.04 são, respectivamente,
O comando que pode ser executado para acessar a ferramenta mencionada é
O limite útil de operação, em metros, para cada ligação de rede com cabo CAT5e é de
Qual a principal ação a ser tomada para minimizar os impactos dos ransomware?
Qual será a maior taxa teórica de download da internet, em Mbps, percebida pelos dispositivos conectados por meio do repetidor?