Questões de Concurso
Foram encontradas 7.137 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A respeito de transferência de calor, mudanças de estado e calorimetria, julgue o item que se segue.
Considere que a temperatura do petróleo extraído em uma
bacia terrestre seja igual a 110 °C. Nesse caso, se esse
petróleo for bombeado por meio de longas tubulações
metálicas até chegar aos tanques de armazenamento, o
petróleo não trocará calor com o meio externo.
Caso o petróleo extraído de um poço esteja armazenado em um tanque metálico por um tempo longo e suficiente para que esse petróleo esteja em equilíbrio térmico com as paredes do tanque e o meio externo, então, nessa situação, não haverá trocas de energia térmica entre o petróleo e o meio externo.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue o próximo item.
Quanto mais eletropositivo um elemento for, maior será sua
tendência de ganhar elétrons.
A respeito das reações de oxirredução e dos ensaios não destrutivos, julgue os próximos itens.
A inspeção visual, ensaio não destrutivo, envolve a
observação direta da superfície do material.
Acerca de funções químicas, julgue o item a seguir.
Bases são caracterizadas pela liberação de íons OH−
e serão
tão mais fortes quanto mais estáveis forem suas fases não
ionizadas.
Acerca de funções químicas, julgue o item a seguir.
Os ácidos fortes são aqueles que se ionizam completamente
em solução aquosa, liberando todos os seus íons H+
, tendo
alta capacidade de doar prótons (íons H+
).
Acerca de funções químicas, julgue o item a seguir.
O potencial de neutralização de um ácido forte é maior em
um ácido fraco que em uma base forte.
Julgue o item a seguir, a respeito de dilatação térmica.
Para um material isotrópico, o coeficiente de dilatação
volumétrico (y) se relaciona com o coeficiente de dilatação
linear (a) por meio da equação 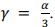
Uma estratégia que permite retirar as tampas metálicas de conservas de vidro é o resfriamento da tampa, se o coeficiente de dilatação linear da tampa metálica for superior ao do vidro.
Julgue o seguinte item, em relação à eletroquímica.
O potencial da semirreação representada a seguir não depende do pH.
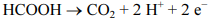
Julgue o seguinte item, em relação à eletroquímica.
Os potenciais-padrão das semirreações de oxirredução são
medidos com base no eletrodo-padrão de hidrogênio, cujo
valor estabelecido é 0,00 V.
Julgue o seguinte item, em relação à eletroquímica.
Considerando-se os potenciais de redução 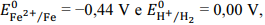 é correto afirmar que
um prego de ferro colocado em uma solução de HCl 1 mol/L
permanece em seu estado inalterado.
é correto afirmar que
um prego de ferro colocado em uma solução de HCl 1 mol/L
permanece em seu estado inalterado.
Segundo a IUPAC, a dupla barra vertical na notação das pilhas eletroquímicas representa a ponte salina.
“O presidente da Belarus, Alexander Lukashenko, afirmou que as nações que estão dispostas a ‘se juntar ao Estado da União da Rússia e da Belarus’ receberão armas nucleares. A utilização de armas nucleares ainda preocupa o mundo, já que estes dispositivos liberam enormes quantidades de energia de maneira explosiva, por meio de reações de fissão nuclear ou de fissão nuclear e fusão nuclear combinadas”.
Adaptado de: https://www.cnnbrasil.com.br/internacional/lukashenko-oferece-armas-nucleares-a-nacoes-dispostas-a-integrar-estado-da-uniao-da-russia-e-da-belarus/
Podemos dizer que os átomos são formados apenas por prótons, elétrons e nêutrons, sob a ótica quântica. Dessa maneira, assinale a alternativa que contém o nome do descobridor de cada partícula atômica, respectivamente:
Considerando a equação de equilíbrio a 160 °C
PCl5(g) ←→ PCl3(g) + Cl2(g)
Foi realizado um experimento, à mesma temperatura, e após o equilíbrio determinaram-se as seguintes concentrações:
[PCl5] = 0,027 mol.L-1
[PCl3] = 0,046 mol.L-1
[Cl2] = 0,012 mol.L-1
Desse modo, pode-se dizer que o valor da constante Kc corresponde, aproximadamente, a:
“Em uma solução ácida a concentração de íons hidrogênio (hidrônio) é maior do que a de íons hidróxido”.
Considerando uma solução de HCl de concentração 4,6.10-3 mol.L-1 (log 4,6 = 0,66), a alternativa que indica o pH e o pOH corretamente é:
(RUSSEL, Química Geral, vol. 2, Editora Pearson, 1994)
Os alcenos podem apresentar isômeros geométricos devido a sua ligação dupla entre átomos de carbono. “A ausência de rotação em torno da ligação dupla carbono-carbono tem consequências químicas, além do interesse teórico”. Quando os carbonos das ligações duplas possuem apenas dois tipos de substituintes, usa-se a nomenclatura cis-trans para diferenciar seus isômeros. Para os carbonos das ligações duplas trissubstituídas e tetrassubstituídas, usa-se o sistema de nomenclatura E, Z, proveniente dos termos alemães entgegen e zusammen. Considerando as duas estruturas a seguir, os nomes corretos a serem atribuídos, respectivamente, são:
(MCMURRY, Química Orgânica.Editora Cengage Learning, 2011)
O Brasil já possui quase 5.000 tipos de agrotóxicos liberados pelo governo federal, por meio do Ministério da Agricultura, Pecuária e Abastecimento. Leia, a seguir, uma notícia veiculada sobre a liberação de agrotóxicos em 2021.
APÓS NOVO RECORDE, BRASIL ENCERRA 2021 COM 562 AGROTÓXICOS LIBERADOS, SENDO 33 INÉDITOS
Registros de defensivos cresceram 14% em relação a 2020. Aprovações vêm aumentando desde 2016.
O Brasil encerrou 2021 com 562 agrotóxicos liberados, maior número da série histórica iniciada em 2000 pelo Ministério da Agricultura. Ainda em dezembro, o total de aprovações já tinha superado o recorde de 2020.
As últimas liberações de 2021 foram publicadas em janeiro no Diário Oficial da União (DOU).
O volume foi 14% superior ao de 2020, quando 493 pesticidas foram autorizados. Os registros vêm crescendo ano a ano no país desde 2016.
https://g1.globo.com/economia/agronegocios/noticia/2022/01/18/apos-novo-recorde-brasilencerra-2021-com-562-agrotoxicos-liberados-sendo-33-ineditos.ghtml
O glifosato é o agrotóxico mais vendido no Brasil. Ele é um herbicida sistêmico de amplo espectro e dessecante de culturas. Suas fórmulas estrutural e molecular são apresentadas abaixo:
C3H8NO5P
Considerando a estrutura apresentada, a alternativa que contém corretamente as funções orgânicas presentes na sua estrutura molecular é:
Um estudante, em laboratório, e utilizando corretamente equipamentos de proteção individual, organizou todos os reagentes e vidrarias necessários para realizar uma titulação. Em um Erlenmeyer, ele adicionou 25 mL de uma solução de ácido oxálico, H2C2O4, que possui dois hidrogênios ionizáveis. Na bureta, o titulante por ele utilizado foi o NaOH(aq) com concentração 0,1 mol.L-1. Ao realizar, cuidadosamente, a titulação, o ponto estequiométrico foi atingido após a adição de 38 mL da solução básica. Portanto, a concentração em mol.L-1 do ácido oxálico é:
“Os compostos de coordenação estão presentes na maioria dos processos químicos que envolvem espécies inorgânicas em temperaturas não muito elevadas. Sob o ponto de vista de estabilidade térmica, alguns são estáveis apenas em baixas temperaturas e outros mantêm suas identidades mesmo a altas temperaturas, podendo, até ser volatilizados. Alguns dos que têm elementos de transição como átomo central são paramagnéticos, enquanto os que têm elementos representativos como átomo central são sempre diamagnéticos. Além disso, muitos dos que se formam pelos metais de transição são coloridos; já os formados pelos elementos representativos são brancos, a não ser que se formem com ligantes coloridos”. A alternativa que associa cada composto ao seu nome de forma CORRETA é:
(FARIAS, Química de Coordenação: fundamentos e atualidades, Editora Átomo, 2009)
I - [Ag(NH3)2]+ |
A - Triacetonitrilatriclorocobalto (Ill) |
II - [Co(NH3)6]3+ |
B - Tetracianoplatinato (II) |
III - [Ag(NH3)2]Cl |
C - Hexaminocobalto (III) |
IV - [Co(an)3Cl3] |
D - Cloreto de diaminoprata (I) |
V - [Pt(Cn)4]2- |
E - Diaminoprata (I) |