Questões de Concurso
Para sesau-al
Foram encontradas 3.614 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
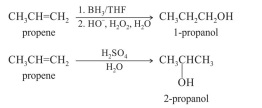
Considerando as informações apresentadas, julgue o item subsequente.
O produto obtido na reação de hidroboração, na presença de
hidróxido de sódio e água oxigenada, do 4-fenil-2-metilbut1-eno é o 4-fenil-2metilbutan-1-ol.

Considerando as informações apresentadas, julgue o item subsequente.
A reação de hidroboração do propano pode ser classificada
como uma reação de adição eletrofílica.

Considerando as informações apresentadas, julgue o item subsequente.
Na oximercuriação seguida de redução para os alcenos, o
produto obtido segue a regra de Markovnikov, desta forma
podemos concluir que na reação do 2-metilpent-2-eno, o
produto formado é o 2-metilpentan-3-ol.

Considerando as informações apresentadas, julgue o item subsequente.
O produto obtido na reação de hidroboração do propano
seguiu a regra de Markovnikov.
O bicarbonato de sódio é comumente utilizado como antiácido estomacal para aliviar a sensação de mal estar após a ingestão de grande quantidade de alimentos, por exemplo. Sabendo que um adulto tem, em média, 100 mL de suco gástrico e que a concentração de ácido clorídrico é de 0,01 mol/L, julgue o item seguinte.
O ponto estequiométrico dessa titulação de neutralização
ocorre com um pH < 7.
O bicarbonato de sódio é comumente utilizado como antiácido estomacal para aliviar a sensação de mal estar após a ingestão de grande quantidade de alimentos, por exemplo. Sabendo que um adulto tem, em média, 100 mL de suco gástrico e que a concentração de ácido clorídrico é de 0,01 mol/L, julgue o item seguinte.
Caso a quantidade de suco gástrico fosse reduzida pela
metade, a massa de bicarbonato utilizada para neutralizar
também deveria ser reduzida pela metade.
O bicarbonato de sódio é comumente utilizado como antiácido estomacal para aliviar a sensação de mal estar após a ingestão de grande quantidade de alimentos, por exemplo. Sabendo que um adulto tem, em média, 100 mL de suco gástrico e que a concentração de ácido clorídrico é de 0,01 mol/L, julgue o item seguinte.
A massa de bicarbonato de sódio necessária para neutralizar
os 100 mL de suco gástrico é de 0,84 g, considerando-se que
o antiácido estomacal tem 80% de pureza de bicarbonato de
sódio na sua composição.
O bicarbonato de sódio é comumente utilizado como antiácido estomacal para aliviar a sensação de mal estar após a ingestão de grande quantidade de alimentos, por exemplo. Sabendo que um adulto tem, em média, 100 mL de suco gástrico e que a concentração de ácido clorídrico é de 0,01 mol/L, julgue o item seguinte.
A reação entre o bicarbonato de sódio e o ácido clorídrico
pode ser classificada como neutralização.
Tendo as informações apresentadas como referência, julgue o item que se segue.
O clorofórmio, solvente orgânico que já foi usado como
anestésico, possui alto grau de toxicidade e pode ser obtido
pela reação de substituição do metano.
Tendo as informações apresentadas como referência, julgue o item que se segue.
O metano (CH4) é um combustível menos poluente que a
gasolina (C8H18) quando se leva em consideração a
combustão completa de 1 kg destes combustíveis.
Tendo as informações apresentadas como referência, julgue o item que se segue.
A reação de formação do clorometano é classificada como
uma reação de substituição via radical que ocorre em três
etapas.
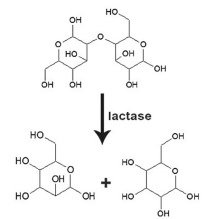
Tendo o texto e a figura precedentes como referência, julgue o item a seguir.
A lactase é a enzima que digere a lactose, que, por sua vez, é
um composto orgânico formado apenas por ametais.

Tendo o texto e a figura precedentes como referência, julgue o item a seguir.
A ligação glicosídica na molécula de lactose é formada pela
ligação β entre o carbono 1 da glicose e o carbono 3 da
galactose.

Tendo o texto e a figura precedentes como referência, julgue o item a seguir.
A molécula de lactose é formada por ligações sigma e pi
entre os átomos.

Tendo o texto e a figura precedentes como referência, julgue o item a seguir.
A glicose e a galactose na forma cíclica são classificadas
como estereisômeros, já que possuem carbonos quirais na
sua estrutura.

Tendo o texto e a figura precedentes como referência, julgue o item a seguir.
A fórmula química da lactose é C12H22O11.
Com relação a esse estudo hipotético, julgue o próximo item.
Quanto maior a concentração dos taninos, menor a
palatabilidade das folhas da espécie em estudo.
Com relação a esse estudo hipotético, julgue o próximo item.
Os flavonoides, de fato, não seriam encontrados no estudo
em questão, pois são metabólitos exclusivos de raízes e
caules.
Com relação a esse estudo hipotético, julgue o próximo item.
A espécie em estudo deve possuir grande ação
anti-inflamatória, devido à presença de cumarinas, que são
metabólitos secundários da classe dos polifenóis.
Com relação a esse estudo hipotético, julgue o próximo item.
Saponinas são glicosídeos do metabolismo secundário
vegetal, caracterizados pela formação de espuma.