Questões de Concurso
Para professor - química
Foram encontradas 4.164 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. No ciclo do carbono o gás carbônico na forma de gás é absorvido pelos vegetais durante a fotossíntese para formar a massa vegetal. II. Já os seres humanos e todos os demais seres vivos, ao respirarem, tanto aeróbica como anaerobicamente, liberam gás carbônico e energia, que pode ser aproveitada de diversas formas, inclusive por outros organismos. III. As reações de dissolução do gás carbônico em água são reações de equilíbrio, em fase líquida aquosa. Essas reações em equilíbrio podem participar de mecanismos de transporte de gás carbônico em meios aquosos tão diferentes como os que existem nos oceanos e do transporte de CO2 entre células e pulmões feito pelo sangue. IV. Os mesmos equilíbrios interagindo com íons metálicos podem resultar na formação de esqueletos e carapaças de organismos como conchas, casca de ovos ou na formação e dissolução de rochas e sedimentos. V. O ser humano interfere globalmente no ciclo do carbono adicionando quantidades significativas de gás carbônico na atmosfera, quando utiliza qualquer combustível contendo carbono proveniente de fonte não renovável.
Assinale a alternativa correta:
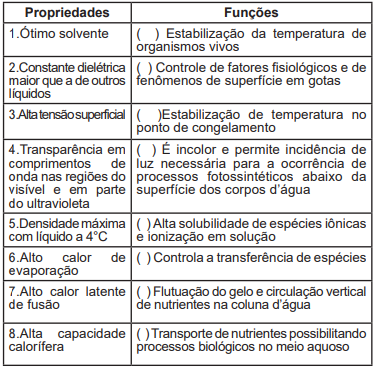
Assinale a alternativa que corresponde à ordem correta das correlações das propriedades com as funções, de cima para baixo segundo o que foi preenchido no quadro anterior:
I. Segundo a teoria de Brønsted-Lowry, o íon bicarbonato na Reação 1 é um ácido. II. Segundo a teoria de Lewis, a amônia na Reação 2 é uma base, pois ela doa elétrons. III. Segundo a teoria de Lewis, o íon bicarbonato na Reação 1 é anfótero. IV. Segundo Brønsted-Lowry, o íon carbonato na Reação 1 é uma base, chamada de base conjugada do íon bicarbonato. V. Todas as bases de Brønsted-Lowry mostradas nas equações são também consideradas bases de Lewis.
Assinale a alternativa correta:
I. As reações não vão até o fim. Elas continuam até que a composição da mistura reacional corresponda ao mínimo de entalpia. Essa composição é descrita por uma constante de equilíbrio característica da reação que depende da temperatura, dentre outros fatores. II. Para controlar o rendimento de uma reação, precisamos entender a base termodinâmica do equilíbrio e como a posição atual de equilíbrio é afetada por condições como a temperatura e a pressão, por exemplo. III. O equilíbrio químico é o estágio da reação química em que não existe mais tendência a mudar a composição da mistura da reação, isto é, as concentrações ou pressões parciais dos reagentes e produtos. Como os equilíbrios físicos, todos os equilíbrios químicos são dinâmicos, com a reação direta e inversa ocorrendo com a mesma velocidade. IV. A termodinâmica descreve quantitativamente o equilíbrio, o que nos possibilita controlar a direção e o rendimento das reações. V. A composição de uma mistura de reação no equilíbrio é descrita pela constante de equilíbrio, que é dependente do produto das atividades dos produtos (elevadas a potências iguais aos coeficientes estequiométricos da equação química balanceada da reação) dividido pelo produto das atividades dos reagentes (elevadas a potências iguais a seus coeficientes estequiométricos).
Assinale a alternativa correta:
Assinale a alternativa correta:
Assinale a alternativa correta:
Assinale a alternativa correta:
I. São favorecidas por solventes polares próticos. II. Podem resultar em misturas de isômeros ópticos. III. Podem apresentar como produtos secundário alcenos. IV. Podem ser mono ou bimoleculares. V. Podem apresentar rearranjos.
Assinale a alternativa correta:
Assinale a alternativa correta:
Assinale a alternativa correta:
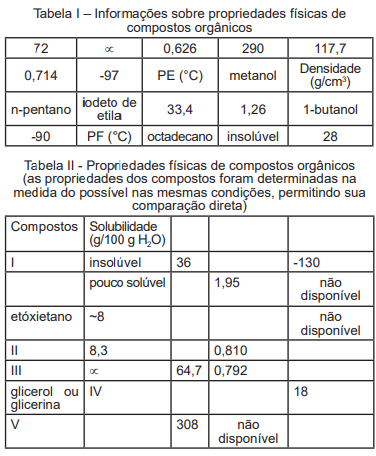 I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta:
I. Sabendo-se que o composto I tem densidade de
0,626 g/cm3
, a menor densidade da lista de compostos
apresentados, ele certamente representa o n-pentano,
pois tal composto possui também baixo ponto de
ebulição e é insolúvel em água.
II. O composto II representa o n-butanol e seu ponto de
fusão é -97°C.
III. O composto III representa o metanol e sua mais alta
solubilidade em relação ao n-butanol está relacionada a
sua maior interação por ligação de hidrogênio, já que a
molécula é menor.
IV. A glicerina ou glicerol (também conhecida como 1, 2, 3-
propanotriol) tem ponto de ebulição muito alto, 290°C,
devido aos grupos hidroxila, mesmo motivo que deixa
este composto extremamente solúvel em água. Assim
sendo, IV representa o símbolo do infinito.
V. O composto V é sólido à temperatura ambiente de 25°C. Assinale a alternativa correta: *Grupo farmacofórico é o conjunto de características eletrônicas e estéricas que caracterizam um ou mais grupos funcionais ou subunidades estruturais, necessários ao melhor reconhecimento molecular pelo receptor e, portanto, para o efeito farmacológico desejado
Assinale a alternativa correta:
Considere a tabela abaixo para responder a questão 38.
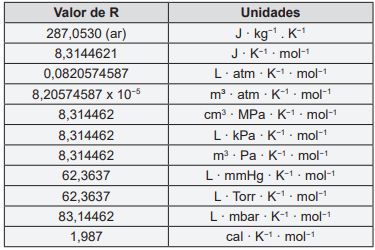
Massas atômicas (u): C = 12,01, O = 16,00, H = 1,01
Analise as seguintes afirmativas e a seguir assinale a alternativa correta:
I. Um tanque de oxigênio armazenado fora de um edifício tem uma pressão de 20,00 atm às 6:00 h da manhã, quando a temperatura está em torno de 10°C. A pressão no tanque às 18:00 h quando a temperatura chega a 30°C é 21,41 atm.
II. Um motor de automóvel mal ajustado pode liberar, em marcha lenta, até 1,00 mol de monóxido de carbono por minuto. A 27°C, o volume desse gás, a 1 atm de pressão que pode ser liberado por minuto é 24,61 L.
III. O óleo produzido a partir de folhas de eucalipto contém o composto volátil eucaliptol. Esse composto tem densidade 0,320 g L-1 a 190°C e 60,0 mmHg. A massa molar do eucaliptol gasoso é 153,89 g mol-1.
IV. O volume de gás carbônico (a 25°C e 1 atm) necessário para que uma planta produza 1,00 g de glicose (C6H12O6) por fotossíntese é 815 mL.
V. A composição do ar seco, em volume, é: 78% de nitrogênio, 21% de oxigênio e 1% de argônio. As pressões parciais desses gases no ar a uma pressão atmosférica de 1 atm são respectivamente, p(N2) = 0,78 atm, p(O2) = 0,21 atm e p(Ar) = 0,01 atm.
Assinale a alternativa correta:
Utilize os dados abaixo para responder a questão 37.

Escreva as semi-reações de cátodo e ânodo e a equação balanceada para os sistemas representados a seguir. Em cada caso faça um esquema da célula galvânica, calcule o valor de ΔE° e determine se corresponde a uma pilha ou eletrólise. Na sequência, assinale a alternativa correta.
Sistemas:
I. Pt(s) | Fe2+(aq), Fe3+(aq) | | Ag+(aq) | Ag(s)
II. Pt(s) | Cl- (aq) | Cl2(g) | | H+(aq) | H2(g) | C(gr)
III. V(s) | V2+(aq) | | U3+(aq) | U(s)
IV. Hg(l) | Cl- (aq) | Hg2Cl2(s) | | Sn4+(aq), Sn2+(aq) | Pt(s)
Assinale a alternativa correta:
: