Questões de Concurso
Para professor - química
Foram encontradas 4.164 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
 , é possível esperar
, é possível esperarNa determinação do teor de acidez de uma amostra de suco de laranja comercial, 10,00 mL de amostra foram levados para erlenmeyer. Adicionou-se água destilada até completar cerca de 50 mL, 3 gotas de fenolftaleína e titulou-se contra solução padrão de NaOH até mudança de coloração. Na titulação, foram gastos 3,90 mL de solução padrão 0,100 mol.L-1.
A acidez é expressa em termos do teor (porcentagem massa/volume) de ácido cítrico, cuja fórmula estrutural é apresentada a seguir.
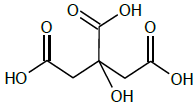
Assinale a opção que expressa a acidez da amostra.
Dados. Massa molar. Ácido Cítrico: 192 g.mol-1.
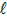 : 74,5; BaSO4: 233
: 74,5; BaSO4: 233“Após a descoberta do elétron, não seria possível ainda conceber um átomo como uma esfera rígida, indivisível, mas como uma esfera ou nuvem de carga positiva, na qual os elétrons estariam embebidos, uniformemente distribuídos.”
Esse conceito de átomo é atribuído a
O cloreto de tionila, composto inorgânico com a fórmula SOC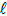 2 ,
é um reagente químico muito usado em reações de cloração. É
um líquido incolor, destilável à temperatura ambiente que
decompõe-se acima de 140ºC. É um composto de S(IV) formado
por ligações químicas de natureza covalente.
2 ,
é um reagente químico muito usado em reações de cloração. É
um líquido incolor, destilável à temperatura ambiente que
decompõe-se acima de 140ºC. É um composto de S(IV) formado
por ligações químicas de natureza covalente.
Assinale a opção que melhor representa a estrutura geométrica
de equilíbrio do cloreto de tionila.
A fórmula a seguir representa o ácido
7-[(1R,3R)-3-hidróxi-2-[(1E,3S)-3-hidróxi-oct-1-en-1-il] -5-oxo-ciclopentil]heptanoico,
foi uma das primeiras substâncias utilizadas para a impotência masculina. Os fármacos que possuíam esta droga na formulação deveriam ser injetados, o que tornava sua utilização inconveniente.
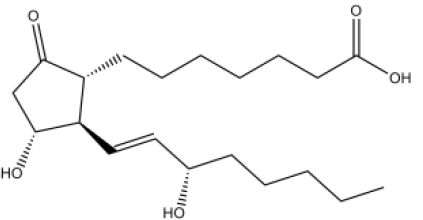
Analisando a nomenclatura e a fórmula desse ácido, é correto
afirmar que seus isômeros
Cientistas identificaram por meio de métodos cromatográficos que o extrato das folhas de lotus possui alcaloides com efeito psicotrópico. O extrato analisado foi administrado em cobaias e apresentou efeitos que superam os de ansiolíticos atualmente utilizados, com a vantagem de apresentar menos efeitos colaterais.
Entre os alcaloides identificados estão:
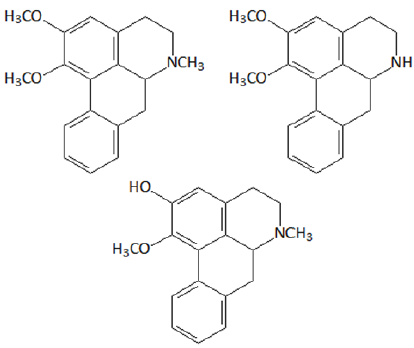
Assinale a opção que indica as funções orgânicas caracterizadas pelos grupos funcionais presentes nessas moléculas.
Nos atentados que ocorreram na cidade de Paris em 2015 os terroristas utilizaram o triperóxido de triacetona, o TATP, uma molécula altamente instável que pode ser detonada com facilidade e cuja está representada a seguir.
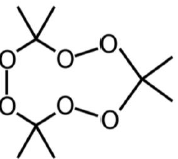
Esta molécula é obtida pela reação da acetona com água oxigenada e, portanto, não contém nitrogênio, tornando mais fácil a sua passagem por dispositivos de segurança que detectam compostos nitrogenados.
Na reação de síntese do TATP citada no enunciado, os carbonos
A análise da concentração de ortofosfato em corpos d’água pode ser feita utilizando o método colorimétrico. Nesse método, o reagente combinado contendo K(SbO)C4H4O6, (NH4)6Mo7O24 e ácido ascórbico reage em meio ácido com o ortofosfato, produzindo uma cor azul, cuja intensidade é determinada no espectrofotômetro.
No preparo de 100 mL do reagente combinado utiliza-se 5 mL de uma solução de K(SbO)C4H4O6 3,5 g.L-1 e 15 mL de uma solução de (NH4)6Mo7O24 40 g.L-1.
Nessa solução do reagente combinado as concentrações
aproximadas (em g.L-1 ) de K(SbO)C4H4O6 e de (NH4)6Mo7O24 são,
respectivamente,
Para quantificar sulfato em uma amostra adequadamente preparada foi elaborada uma curva de calibração a partir da diluição de uma solução padrão com concentração 100,0 mg.L-1 . A curva de calibração utilizou as seguintes soluções:
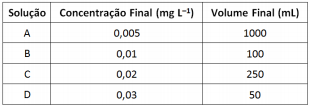
Sobre as soluções preparadas são feitas as afirmativas a seguir.
I. Para preparar as soluções A e C foram utilizados os mesmos volumes da solução padrão.Sobre as soluções preparadas são feitas as afirmativas a seguir.
II. Para preparar a solução B foi utilizado o menor volume da solução padrão.
III. Para preparar a solução D foi utilizado o maior volume da solução padrão.
Está correto o que se afirma em
Um técnico preparou em um balão volumétrico 250 mL de uma solução diluída de ácido clorídrico (a 20ºC), pipetando adequadamente 8,4 mL do ácido concentrado 37% m/m de densidade 1,19 g.cm-3 (a 20ºC).
A concentração da solução preparada, em mol.L-1 é de, aproximadamente,
Dados: Massas molares: H = 1g.mol-1 Cl = 35,5 g.mol-1
O fósforo é absorvido pelas plantas na forma de ânions; um desses ânions é o (H2PO4 )- derivado da fluorapatita, encontrada em rochas.
A fluorapatita, representada como Ca5 (PO4 )3F, é insolúvel em água e é convertida a di-hidrogenofosfato de cálcio através da reação não balanceada:
Ca5 (PO4 )3F (s) + H2SO4 (aq) → Ca(H2PO4)2 (aq) + CaSO4 (aq) + HF (g)
A soma dos menores coeficientes inteiros que balanceiam esta
equação é
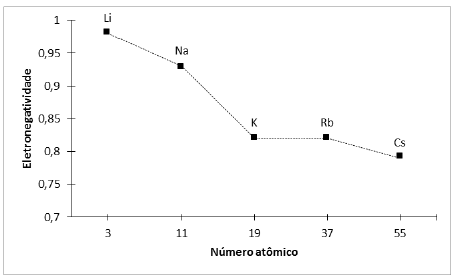
De acordo com os dados apresentados, o metal alcalino que estabelecerá com o flúor a ligação química de maior caráter iônico será o
O posicionamento dos metaloides entre os metais e os não-metais é o nosso primeiro exemplo das tendências na variação das propriedades quando nos deslocamos na tabela periódica. Frequentemente veremos que, à medida que mudamos de posição em um período ou em um grupo, as propriedades físicas e químicas variam de modo mais ou menos regular. Há poucas variações abruptas nas características dos elementos quando nos deslocamos horizontalmente ao longo de um período ou verticalmente através de um grupo.
(Brady, J.; Senese, F. Química a matéria e suas transformações Vol 1, 5ª Ed. Rio de janeiro: LTC. 2009)
Com relação aos raios dos átomos, analise as afirmativas a seguir.
I. O raio do ferro é menor que o raio do potássio.
II. O raio do paládio é maior que o raio do níquel.
III. O raio do manganês e maior que o raio do estrôncio
Está correto o que se afirma em
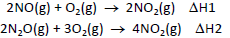
A variação de entalpia da reação N2O(g) + 1/2O2 (g) → 2NO(g) pode ser determinada como
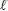 )
) Esta reação, descoberta pelo químico francês Paul Sabatier, tem sido estudada para remover CO2 de atmosferas artificiais como em espaçonaves. Considerando que um indivíduo libere para o ambiente 0,6 kg de dióxido de carbono por dia, e que 80% desse gás será removido pelo processo de Sabatier, a massa de metano produzida por dia é de Dados: Massas Molares: H = 1g.mol-1 C = 12g.mol-1 O=16g.mol-1