Questões de Concurso
Para técnico em química
Foram encontradas 870 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
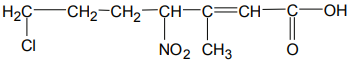
O nome IUPAC para o seguinte composto é:
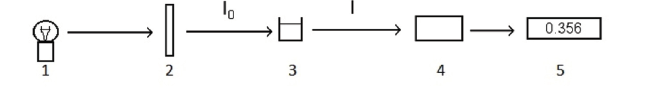
Baseado no diagrama apresentado, escolha a alternativa INCORRETA
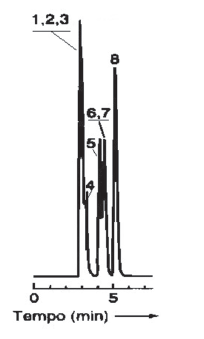
Em relação ao seguinte cromatograma gasoso, obtido isotermicamente, a 70 °C, em uma coluna capilar apolar de 40 metros, com um detector de ionização de chama (DIC), é INCORRETO afirmar que
A figura abaixo ilustra a eluição de uma amostra e de duas substâncias puras, a e B, em uma cromatoplaca. Antes da Eluição Após da Eluição

 Frente do eluente
Frente do eluenteDe acordo com a figura, é CORRETO afirmar que
Considere o procedimento a seguir:
Uma massa de 1,0000g de uma amostra contendo cloreto foi dissolvida e transferida quantitativamente para balão volumétrico de 100,0 mL, que teve seu volume completado com água destilada. Uma alíquota de 20,00 mL deste balão foi transferida para um erlenmeyer, ao qual adicionaram-se 30,00 mL de AgNO3 0,0500 mol L-1 para precipitar o AgCl. Após a filtração e lavagem do precipitado, com transferência quantitativa do filtrado para outro erlenmeyer, o excesso de Ag+ foi titulado com 15,00mL de NH4 SCN 0,0500mol L-1.
Em relação à determinação descrita é INCORRETO afirmar que
A reação da glicose (C6 H12O6 ) com o reagente de Tollens ocorre segundo a seguinte reação: C6 H12O6 (aq) + 2 Ag+(aq) + 2 OH- (aq) ⥨ C6 H12O7 (aq) + 2 Ag(s) + H2 O(l)
Em função da reação apresentada, é CORRETO afirmar que
Tabela: solubilidade de A em água a diversas temperaturas Temperatura (°C) 10 20 30 40 50 60 Concentração de A (mg mL-1) 3 6 9 12 15 18
Analisando os dados da tabela, é CORRETO afirmar que
a I2 O5 (s) + b CO(g) ⥨ c I2 (g) + d CO2 (g) e I2 (aq) + f S2 O3 2-(aq) ⥨ g I- (aq) + h S4 O6 2-(aq)
Após balanceadas as equações, é CORRETO afirmar sobre os coeficientes de balanceamento que
I. 100,00 mL de ácido acético (CH3 COOH) 0,124 mol L-1 (pKa = 4,74) com 25,00 mL de hidróxido de potássio (KOH) 0,248 mol L-1. II. 50,00 mL de hidróxido de amônio (NH4 OH) 0,02 mol L-1 (pKb = 4,74) com 50 mL de cloreto de amônio (NH4 Cl) 0,2 mol L-1. III. 25,00 mL de ácido perclórico (HClO4 ) 0,05 mol L-1com 50,00 mL de hidróxido de potássio (KOH) 0,04 mol L-1.
O problema se deu pelo cálculo errado da quantidade de combustível, devido à recente substituição do sistema imperial pelo sistema métrico. O avião seria considerado corretamente abastecido, caso a massa total de combustível fosse 22300 kg, mas apenas recebeu um total de 22300 libras, menos da metade.
Considerando que o Avião já continha 7712 litros de combustível e que deveria ter um total de 22300 kg de combustível, quantos litros de combustível o avião deveria ter recebido no abastecimento? (Densidade do combustível = 0,800 kg L-1)
I. Laboratório 0,410; 0,445; 0,428 (média = 0,428; desvio padrão = 0,02). II. Laboratório 0,439; 0,320; 0,558 (média = 0,439; desvio padrão = 0,12). III. Laboratório 0,372; 0,373; 0,372 (média = 0,3726; desvio padrão = 0,0006).
Com base nos resultados apresentados, e no teor certificado, é CORRETO afirmar que os resultados