Questões de Concurso
Para química
Foram encontradas 13.134 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
C2O4 2 – + MnO4 1 – + H + → Mn 2 + + H2O + CO2
Após o balanceamento correto, a soma dos coeficientes estequiométricos dos produtos da reação é:
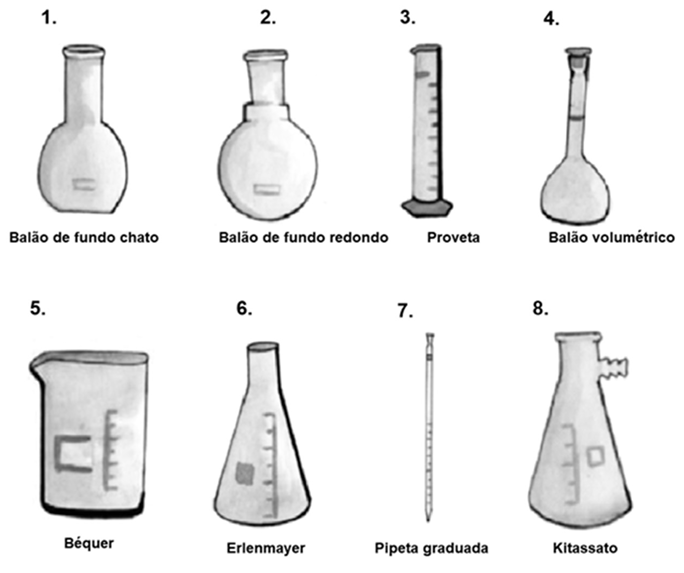
Fonte: Silva et al., 2019.
CLASSIFICAÇÃO DE PERIGO DO PRODUTO (ABNT NBR 14725-2)
Mutagenicidade em células germinativas (Categoria 2)
Carcinogenicidade (Categoria 1B)
Toxicidade reprodutiva (Categoria 2)
ELEMENTOS APROPRIADOS DA ROTULAGEM (ABNT NBR 14725-3)
Pictogramas:

Palavra de Advertência: Perigo
Frases de Perigo:
341 Suspeito de provocar anomalias genéticas.
H350 Pode provocar cancro.
H361 Suspeito de afetar a fertilidade ou o nascituro.
Frases de Precaução:
P201 Pedir instruções específicas antes da utilização.
P202 Não manuseie o produto antes de ter lido e percebido todas as precauções de segurança.
P281 Usar o equipamento de proteção individual exigido.
P308 + P313 EM CASO DE exposição ou suspeita de exposição: consulte um médico.
P405 Armazenar em local fechado à chave.
P501 Eliminar o conteúdo/ recipiente em instalação aprovada de destruição de resíduos.
Portanto, quando ao técnico for solicitado o preparo de uma solução de fenolftaleína, os seguintes equipamentos devem ser utilizados, EXCETO:
Pode-se obter o bórax anidro (Na2B4O7) através da reação representada pela equação não balanceada:
Ácido bórico + Metaborato de sódio → Na2B4O7 + H2O
A alternativa que apresenta as fórmulas corretas dos reagentes utilizados para sintetizar o bórax é:
De acordo com a legislação atual da ANVISA, RDC 166/2017, os parâmetros de validação de métodos analíticos envolvem Seletividade, Linearidade, Exatidão, Precisão (repetitividade, precisão intermediária e reprodutibilidade), Limite de Detecção (LD), Limite de Quantificação (LQ) e Robustez.
Sabendo que:
b = branco instrumental (coeficiente linear da curva de calibração); Sb = desvio padrão para o branco instrumental; S = sensibilidade do método (coeficiente angular da curva de calibração)
Sobre o Limite de quantificação (LQ), podemos afirmar que
Fonte: https://blog.forlabexpress.com.br/como-funciona-o-rotaevaporador-ou-evaporador-rotativo /#:~:text=O%20evaporador%20rotativo%20funciona%20de,realizando%2C%20assim%2C%20a%20eva pora%C3%A7%C3%A3o. (adaptado) acessado 21/09/2023.
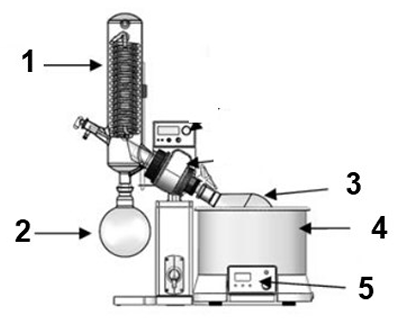
Fonte: https://esp.labbox.com/evaporador-rotativo-todo-lo-que-debes-saber/ adaptado (acessado 29/09/2023).
As setas do rotaevaporador da figura acima indicam, respectivamente:
( ) Quando ácidos entram em contato com as mãos, deve-se lavar com água corrente e, em seguida, neutralizar a acidez remanescente com solução de bicarbonato de sódio.
( ) Quando bases entram em contato com as mãos, deve-se lavar com água corrente e, em seguida, neutralizar a basicidade remanescente com solução de ácido acético ou ácido bórico a 1%.
( ) Quando substâncias de caráter básico entram em contato com os olhos, deve-se lavar com água corrente utilizando lava-olhos e, em seguida, neutralizar a basicidade remanescente com solução de ácido bórico a 1%.
Classificando as afirmações em VERDADEIRAS (V) ou FALSAS (F), a ordem CORRETA obtida, de cima para baixo, é:
I2 + KOH → KI + KIO3 + H2O
Analise as afirmações sobre a reação acima:
( ) O iodo é o agente oxidante e redutor.
( ) Após balanceamento da equação, verifica-se que a soma dos coeficientes estequiométricos é igual em ambos os membros da equação.
( ) O iodo é o agente oxidante e o hidróxido de potássio é o agente redutor.
( ) Os nomes oficiais dos compostos de iodo produzidos são iodeto de potássio e periodato de potássio, respectivamente.
Classificando as afirmações em VERDADEIRAS (V) ou FALSAS (F) a ordem CORRETA obtida, de cima para baixo, é:
Fonte: https://brasilescola.uol.com.br/quimica/Acido-cloridrico.htm (adaptado) acessado 21/09/2023.
Para o teste de bioacessibilidade, um técnico preparou uma solução diluída desse ácido, com concentração 1,0.10 − 8 mol. L− 1. Essa solução apresenta pH, aproximadamente, igual a
( ) Não se deve armazenar ácidos inorgânicos no mesmo espaço onde se armazena sulfeto de ferro (II), pois, caso esses reagentes entrem em contato, há o risco da liberação de um gás tóxico.
( ) Cianeto de potássio pode ser armazenado com ácidos porque não há nenhum risco de produção de substâncias tóxicas se esses reagentes entrarem em contato.
( ) Pode-se armazenar alumínio metálico com hidróxido de potássio porque essas substâncias não reagem entre si.
( ) Metais alcalinos devem ser guardados em recipientes fechados, imersos em substâncias pouco reativas, tais como querosene.
A opção que apresenta a ordem CORRETA da classificação, lida de cima para baixo, é:
Fonte: https://brasilescola.uol.com.br/quimica/gravimetria.htm (adaptado) acessado 21/09/2023.
Uma alíquota de 50 mL de uma solução de ácido sulfúrico reagiu totalmente com uma solução de cloreto de bário, formando 9,32 g de um precipitado branco. Qual a concentração da solução de ácido sulfúrico?
https://www.ecycle.com.br/bom-ou-ruim-usado-como-conservante-em-vinhos-dioxido-de-enxofrepode-causar-reacoes-alergicas/ (adaptado) acessado:2109/2023.
Ao se atacar 1,04 kg de sulfito de magnésio, com ácido clorídrico, qual o volume de anidrido sulfuroso obtido a 27°C e 1869 mmHg?
Fonte: https://www.fop.unicamp.br/index.php/pt-br/normalidade-bioquimica-calculos.html (adaptado) acessado 21/09/2023.
Considerando que foi solicitado o preparo de 500 mL, solução de sulfato de sódio 0,2 Normal, qual a massa do sal necessária para o preparo da solução?
Dermocosméticos com ácido glicólico são eficientes no rejuvenescimento e beleza da pele, pois conseguem promover a renovação celular através da esfoliação e da descamação da pele. Contudo, seu uso deve ser orientado por dermatologistas.
Fonte:https://jornal.usp.br/podcast/pilula-farmaceutica-92-acido-glicolico-deve-estar-emconcentracoes-ideais-para-evitar-lesoes-na-pele/ (adaptado) acessado: 21/09/2023.
Para o controle de qualidade de uma amostra de ácido glicólico (CH3OCOOH), preparou-se 25,00 mL de solução 0,080 mol L-1, sendo esta titulada e neutralizada com solução padronizada de NaOH 0,100 mol/L. Qual o volume de base utilizado?
Dado: Ka (ácido acético) = 1,8 x 10-5