Questões de Vestibular
Sobre gás ideal em física
Foram encontradas 120 questões

Considere-se que um automóvel movido a H2 (g) possua um reservatório com capacidade para 100 L do gás e apresente um consumo médio de 1,0 kg de H2 a cada 100 km percorridos. Considere-se, também, que, no momento do abastecimento com o gás, o reservatório esteja na temperatura de 300 K. Nessas condições, para que o automóvel possa percorrer 600 km sem necessitar de novo abastecimento, o gás deverá estar armazenado a uma pressão superior a 600 atm.
Use os valores aproximados: g = 10 m/s2 e π = 3.
Uma das etapas mais difíceis de um voo espacial tripulado é a
reentrada na atmosfera terrestre. Ao reencontrar as camadas
mais altas da atmosfera, a nave sofre forte desaceleração e sua
temperatura externa atinge milhares de graus Celsius. Caso a
reentrada não ocorra dentro das condições apropriadas, há risco de graves danos à nave, inclusive de explosão, e até mesmo
risco de ela ser lançada de volta ao espaço.

A partir de certo instante, a parede que separa os compartimentos é removida e, após algum tempo, o sistema atinge uma nova temperatura de equilíbrio Tm. Supondo que não há trabalho realizado após a remoção da parede, nem troca de calor entre o sistema e o ambiente externo, a temperatura de equilíbrio Tm é dada por:
Considere: A constante universal dos gases ideais é R= 8,314 Pa m3/(mol K)
Um mol de um gás ideal percorre o processo cíclico ABCA em um diagrama P-V, conforme mostrado na figura, sendo que a etapa AB é isobárica, a etapa BC é isocórica e a etapa CA é isotérmica.
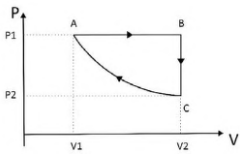
Considere as seguintes afirmações:
I, O gás libera calor tanto na etapa BC quanto na etapa CA,
II, O módulo do trabalho realizado pelo gás é não nulo tanto na etapa AB quanto na etapa BC,
III, O gás tem sua temperatura aumentada tanto na etapa AB quanto na etapa CA,
É correto o que se afirma em:

A figura precedente mostra um diagrama pressão versus volume que corresponde a uma transformação cíclica sofrida por um gás ideal. O ciclo é percorrido na seguinte sequência: A → B, B → C, C → D, D → A.
A respeito do diagrama, e considerando que 1 bar = 10 5 Pa e que 1 L = 10 -3 m 3 , julgue o próximo item.
No ciclo termodinâmico completo, o trabalho realizado pelo gás é igual a 100 J.

A figura precedente mostra um diagrama pressão versus volume que corresponde a uma transformação cíclica sofrida por um gás ideal. O ciclo é percorrido na seguinte sequência: A → B, B → C, C → D, D → A.
No ciclo termodinâmico completo, a variação de energia interna do gás é nula.
As descrições dos processos I e II e a avaliação das variações de energia interna correspondem a:
Um gás ideal contido em um cilindro com pistão pode ser levado de um estado inicial i até um estado final f, seguindo dois processos distintos, I e II, conforme ilustrado na figura abaixo.

Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem.
No processo I, o gás sofre duas transformações sucessivas, sendo a primeira ........ e a segunda ........ .
A variação de energia interna no processo I, ∆UI, é ........ variação de energia interna no processo II, ∆UII.
Um gás ideal contido em um cilindro com pistão pode ser levado de um estado inicial i até um estado final f, seguindo dois processos distintos, I e II, conforme ilustrado na figura abaixo.

Considere as afirmações abaixo, sobre o comportamento térmico dos gases ideais.
I - Volumes iguais de gases diferentes, na mesma temperatura inicial, quando aquecidos sob pressão constante de modo a sofrerem a mesma variação de temperatura, dilatam-se igualmente.
II - Volumes iguais de gases diferentes, na mesma temperatura e pressão, contêm o mesmo número de moléculas.
III- Uma dada massa gasosa, quando mantida sob pressão constante, tem temperatura T e volume V diretamente proporcionais.
Quais estão corretas?