Questões de Vestibular
Sobre gás ideal em física
Foram encontradas 115 questões

Glossário de Matemática
sen 30° =5 cos 30°= √3/2 ≈0,9 sen 60° = √3/2 ≈0,9
sen 45°= √2/2 ≈0,7 cos 45°= √2/2 ≈0,7 cos 60° = 0,5
Deve-se considerar para todos os problemas
c = 3,0 x 108 m/s vsom = 340m/s g = 10m /s2 G = 6 x 10-11 N.m2 /Kg2
R = 0,08atm.L / mol.K h = 6 x 10-34 J.s 1eV = 1,6 x 10-19 J
Certa quantidade de gás ideal ocupa inicialmente um volume V0 , à pressão p0 e temperatura T0 . Esse gás se expande à temperatura constante e realiza trabalho sobre o sistema, o qual é representado nos gráficos pela área sob a curva.
Assinale a alternativa que melhor representa a variação de energia.
Um gás ideal contido em um cilindro com pistão pode ser levado de um estado inicial i até um estado final f, seguindo dois processos distintos, I e II, conforme ilustrado na figura abaixo.

Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem.
No processo I, o gás sofre duas transformações sucessivas, sendo a primeira ........ e a segunda ........ .
A variação de energia interna no processo I, ∆UI, é ........ variação de energia interna no processo II, ∆UII.
Um gás ideal contido em um cilindro com pistão pode ser levado de um estado inicial i até um estado final f, seguindo dois processos distintos, I e II, conforme ilustrado na figura abaixo.

Considere as afirmações abaixo, sobre o comportamento térmico dos gases ideais.
I - Volumes iguais de gases diferentes, na mesma temperatura inicial, quando aquecidos sob pressão constante de modo a sofrerem a mesma variação de temperatura, dilatam-se igualmente.
II - Volumes iguais de gases diferentes, na mesma temperatura e pressão, contêm o mesmo número de moléculas.
III- Uma dada massa gasosa, quando mantida sob pressão constante, tem temperatura T e volume V diretamente proporcionais.
Quais estão corretas?
Antes de viajar, o motorista calibrou os pneus do seu carro a uma pressão de 30psi quando a temperatura dos pneus era de 27ºC. Durante a viagem, após parar em um posto de gasolina, o motorista percebeu que os pneus estavam aquecidos. Ao conferir a calibragem, o motorista verificou que a pressão dos pneus era de 32psi.
Considerando a dilatação do pneu desprezível e o ar dentro dos pneus como um gás ideal, assinale a alternativa que MELHOR representa a temperatura mais próxima dos pneus.
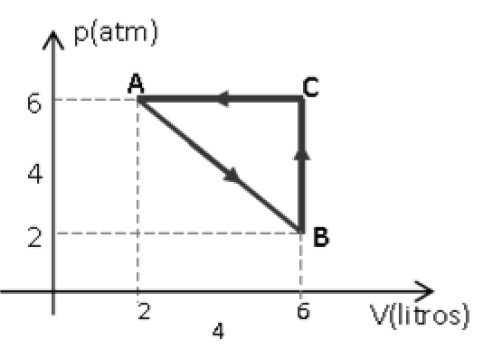
Um gás perfeito realiza o ciclo esquematizado no diagrama de trabalho no sentido ABCA. Determine o valor trabalho, em módulo, realizado no processo A → B → C.
(Dados: 1,0 atm = 105 N/m2 e 1,0 litro = 10-3 m3 ).
Uma amostra de gás ideal está aprisionada em uma seringa de vidro que está em contato térmico com o meio ambiente. Lentamente, o êmbolo é pressionado (sem deixar escapar gás) até que o volume do gás diminui à metade e a sua pressão é dobrada.
Sobre a temperatura T do gás e o sinal do trabalho realizado por ele, nesse processo, conclui-se que
Uma das formas de transformar calor em trabalho é por meio de máquinas térmicas. Um recipiente completamente fechado contendo um gás ideal, em que uma de suas faces, em forma de um êmbolo, possui liberdade de se mover em uma dada direção é um sistema termodinâmico simples que pode servir para exemplificar uma máquina térmica. Nesse exemplo, quando uma fonte de calor fornece energia ao gás, dependendo das condições, as transformações podem fazer com que o êmbolo se mova, realizando um trabalho. Na figura (A), está indicada a situação inicial de um gás ideal em condições de temperatura (T0), volume (V0) e pressão (P0), com o êmbolo recebendo uma resistência externa (R0) e, na figura (B), estão indicadas as condições finais após o gás receber calor, sofrer um aquecimento e uma expansão, com temperatura (TF), volume (VF), pressão (PF) e recebendo uma resistência externa (RF).
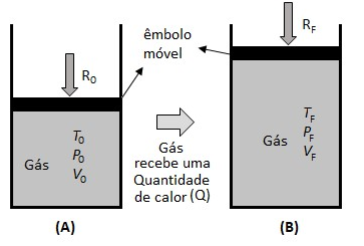
Considerando-se que, no caso da figura, as forças de resistências inicial (R0) e final (RF) são
diferentes, é correto afirmar que
Um peixe ósseo com bexiga natatória, órgão responsável por seu deslocamento vertical, encontra-se a 20 m de profundidade no tanque de um oceanário.
Para buscar alimento, esse peixe se desloca em direção à superfície; ao atingi-la, sua bexiga natatória encontra-se preenchida por 112 mL de oxigênio molecular.
Considere que o oxigênio molecular se comporta como gás ideal, em condições normais de temperatura e pressão. Quando o peixe atinge a superfície, a massa de oxigênio molecular na bexiga natatória, em miligramas, é igual a:
Em um reator nuclear, a energia liberada na fissão de 1 g de urânio é utilizada para evaporar a quantidade de 3,6 x 104 kg de água a 227 ºC e sob 30 atm, necessária para movimentar uma turbina geradora de energia elétrica.
Admita que o vapor d’água apresenta comportamento de gás ideal.
O volume de vapor d’água, em litros, gerado a partir da fissão de 1 g de urânio, corresponde a:
TEXTO 7
Memórias de um pesquisador
Não era bem vida, era uma modorra – mas de qualquer modo suportável e até agradável. Terminou bruscamente, porém, eu estando com vinte e oito anos e um pequeno bujão de gás explodindo mesmo à minha frente, no laboratório de eletrônica em que trabalhava, como auxiliar. Me levaram às pressas para o hospital, os médicos duvidando que eu escapasse. Escapei, mas não sem danos. Perdi todos os dedos da mão esquerda e três (sobraram o polegar e o mínimo) da direita. Além disso fiquei com o rosto seriamente queimado. Eu já não era bonito antes, mas o resultado final – mesmo depois das operações plásticas – não era agradável de se olhar. Deus, não era nada agradável.
No entanto, nos primeiros meses após o acidente eu não via motivos para estar triste. Aposentei-me com um bom salário. Minha velha tia, com quem eu morava, desvelava-se em cuidados. Preparava os pastéis de que eu mais gostava, cortava-os em pedacinhos que introduzia em minha boca – derramando sentidas lágrimas cuja razão, francamente, eu não percebia. Deves chorar por meu pai – eu dizia – que está morto, por minha mãe que está morta, por meu irmão mais velho que está morto; mas choras por mim. Por quê? Escapei com vida de uma explosão que teria liquidado qualquer um; não preciso mais trabalhar; cuidas de mim com desvelo; de que devo me queixar?
Cedo descobri. Ao visitar certa modista.
Esta senhora, uma viúva recatada mas ardente, me recebia todos os sábados, dia em que os filhos estavam fora. Quando me senti suficientemente forte telefonei explicando minha prolongada ausência e marcamos um encontro.
Ao me ver ficou, como era de se esperar, consternada. Vais te acostumar, eu disse, e propus irmos para a cama. Me amava, e concordou. Logo me deparei com uma dificuldade: o coto (assim eu chamava o que tinha me sobrado da mão esquerda) e a pinça (os dois dedos restantes da direita) não me forneciam o necessário apoio. O coto, particularmente, tinha uma certa tendência a resvalar pelo corpo coberto de suor da pobre mulher. Seus olhos se arregalavam; quanto mais apavorada ficava, mais suava e mais o coto escorregava.
Sou engenhoso. Trabalhando com técnicos e cientistas aprendi muita coisa, de modo que logo resolvi o problema: com uma tesoura, fiz duas incisões no colchão. Ali ancorei coto e pinça. Pude assim amá-la, e bem.
– Não aguentava mais – confessei, depois. – Seis meses no seco!
Não me respondeu. Chorava. – Vais me perdoar, Armando – disse – eu gosto de ti, eu te amo, mas não suporto te ver assim. Peço-te, amor, que não me procures mais.
– E quem vai me atender daqui por diante? – perguntei, ultrajado.
Mas ela já estava chorando de novo. Levantei-me e saí. Não foi nessa ocasião, contudo, que fiquei deprimido. Foi mais tarde; exatamente uma semana depois.
[...]
(SCLIAR, Moacyr. Melhores contos. Seleção de
Regina Zilbermann. São Paulo: Global, 2003. p.
176-177.)
I-O gás no interior do botijão está em CNTP.
II- Se o botijão não suportar a pressão interna e explodir, isto pode ser considerado um processo adiabático.
III- Se houver um grande vazamento no botijão, fazendo que a pressão interna caia repentinamente, sua temperatura cairá, podendo formar cristais de gelo nas suas paredes externas.
IV- Supondo-se que um botijão suporte uma pressão interna máxima de 15 atm e que, na temperatura ambiente de 27 ºC, a pressão interna seja igual a 5 atm e todo o seu conteúdo se encontre no estado gasoso, comportando-se como um gás ideal. Nessas condições, então, o botijão explodirá se for aquecido até 427 ºC.
Com base nas sentenças anteriores, marque a alternativa em que todos os itens estão corretos:
O volume de ar, em m3, necessário para essa operação, à pressão atmosférica de 1 atm, é aproximadamente igual a:
Um gás ideal sofre uma compressão isobárica tal que seu volume se reduz a 2/3 do inicial.
Se a temperatura inicial do gás era de 150 °C, a temperatura final, em °C, é:
Gases, vapores e misturas de gases e vapores, quando afastados de seus pontos de liquefação, apresentam um comportamento comum descrito pela equação pV=nRT. Portanto, nas mesmas condições de pressão e temperatura, esses sistemas, para um mesmo volume, apresentarão a mesma quantidade de partículas. Assim, se uma molécula de água ingressar no ar, alguma outra deverá sair.
Aplicando essas considerações para o ar seco (com pouco ou nenhum vapor de água) e para o ar úmido (com vapor de água), afirma-se:
I. O ar úmido é mais denso que o ar seco, pois o vapor de água (H2O) é mais denso do que o ar seco.
II. O ar úmido é menos denso que o ar seco, porque a massa da molécula de água é menor do que a das moléculas de oxigênio (O2 ) e nitrogênio (N2 ).
III. O ar seco é menos denso que o ar úmido, porque apresenta menor quantidade de moléculas.
A(s) afirmativa(s) correta(s) é/são: