Questões de Vestibular
Sobre estudo da matéria: substâncias, misturas, processos de separação. em química
Foram encontradas 247 questões
Considerando as informações do texto, têm-se as seguintes afirmativas: I - O suor é uma mistura heterogênea do tipo suspensão. II - A densidade do suor é a razão entre seu volume e sua massa e representa uma propriedade química. III - O suor sobre a pele desaparece quando o atleta pára de jogar, porque retira energia térmica do corpo para transformar seu estado físico de líquido para gasoso. IV - Os íons sódio e potássio, contidos no suor, são metais alcalinos e pertencem ao primeiro grupo da tabela periódica. V - Os íons sódio, potássio e magnésio, liberados durante a transpiração, possuem cargas iguais a +1, +1 e +2, respectivamente.
Assinale a alternativa que reúne somente afirmativas corretas.
A figura mostra um processo de extração da vanilina a partir de vagens de orquídea espalhadas sobre bandejas perfuradas, em tanques de aço, usando etanol (60% v/v) como solvente. Em geral, a extração dura duas semanas.
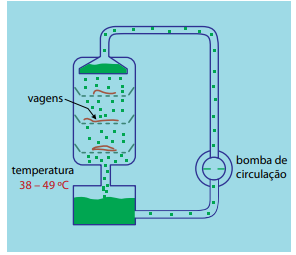
(www.greener-industry.org.uk. Adaptado.)
De acordo com o que mostra a figura, a extração da vanilina a partir de fontes naturais se dá por
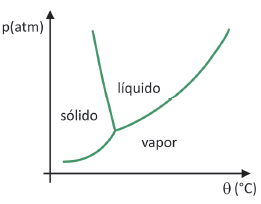
Apesar de ser um processo que requer, industrialmente, uso de certa tecnologia, existem evidências de que os povos pré‐ colombianos que viviam nas regiões mais altas dos Andes conseguiam liofilizar alimentos, possibilitando estocá‐los por mais tempo. Assinale a alternativa que explica como ocorria o processo de liofilização natural:
A primeira lâmpada comercial, desenvolvida por Thomas Edison, consistia em uma haste de carbono, que era aquecida pela passagem de uma corrente elétrica a ponto de emitir luz visível. Era, portanto, uma lâmpada incandescente, que transforma energia elétrica em energia luminosa e energia térmica. Posteriormente, passou-se a utilizar, no lugar da haste, filamentos de tungstênio, cuja durabilidade é maior. Hoje, esse tipo de lâmpada tem sido substituído pelas lâmpadas fluorescentes e de LED.
As lâmpadas fluorescentes são construídas com tubos de vidro transparente revestidos internamente e contêm dois eletrodos (um em cada ponta) e uma mistura de gases em seu interior — vapor de mercúrio e argônio, por exemplo. Quando a lâmpada fluorescente é ligada, os eletrodos geram corrente elétrica, que, ao passar através da mistura gasosa, excita seus componentes, os quais, então, emitem radiação ultravioleta. O material que reveste o tubo tem a propriedade de converter a radiação ultravioleta em luz visível, que é emitida para o ambiente.
A lâmpada de LED é mais econômica que a incandescente, pois dissipa menos energia em forma de calor. Em geral, essas lâmpadas têm eficiência de 15 lumens por watt. Um lúmen (unidade padrão do Sistema Internacional) é o fluxo luminoso emitido por uma fonte puntiforme com intensidade uniforme de 1 candela e contido em um cone de ângulo sólido de um esferorradiano. A tabela a seguir apresenta características específicas das lâmpadas incandescentes, fluorescentes e de LED.

A partir do texto acima e considerando que 6,63 × 10-34 J-s seja o valor da constante de Planck, que 3 × 108 m/s seja a velocidade da luz e que a temperatura em graus Kelvin seja exatamente igual à temperatura em graus Celsius acrescida de 273, julgue o item que é do tipo C.
A mistura de vapor de mercúrio e argônio gasoso é
considerada uma mistura
homogênea.

A partir da polimerização de determinado monômero,
realizada em solução com duas diferentes condições reacionais,
chegou-se a polímeros com diferentes distribuições de
massas molares, conforme ilustrado na figura acima. Ao final
dos procedimentos de síntese, as duas soluções obtidas —
uma contendo o polímero A (solução I) e outra, o polímero B
(solução II) — tinham concentrações iguais, em g/L.
Com base nessa situação e considerando que os comportamentos das soluções sejam ideais e que os polímeros sejam estáveis na temperatura de ebulição do solvente empregado em suas sínteses, julgue o item.
A separação dos polímeros a partir da solução obtida ao final
de cada reação pode ser realizada pelo processo de destilação.
O acetato de etila (CH3COOCH2CH3) é um éster simples, usado, no passado, como antiespasmódico e hoje como solvente industrial e removedor de esmalte de unha. A acetona (CH3(CO)CH3) também é usada como removedor de esmaltes, mas devido a sua elevada solubilidade em água, quando em contato com a pele, pode desidratá-la. Sabe-se que estes solventes possuem cheiros parecidos, tornando difícil a identificação pelo olfato.
Considerando um frasco contendo acetato de etila e acetona em quantidades equimolares, assinale a alternativa que apresenta, corretamente, o procedimento para a separação da mistura.
Dados:
Ponto de ebulição do acetato de etila a 1 atm =77,1 °C e densidade = 902 Kg/m3
Ponto de ebulição da acetona a 1 atm = 56,0 °C e densidade = 784 Kg/m3
Nas prateleiras de supermercados é comum encontrarmos alimentos desidratados, isto é, isentos de água em sua composição. Para desidratar alimentos, é utilizado o processo de liofilização que consiste em se congelar o alimento à temperatura de -197°C e depois submeter o alimento congelado a pressões muito baixas. Na temperatura de -197°C, a água do alimento encontrase na fase sólida e, com o abaixamento de pressão, passa diretamente para a fase de vapor, sendo então eliminada.
Assinale a afirmação CORRETA:

Consideram-se arte rupestre as representações feitas sobre rochas pelo homem da pré-história, em que se incluem gravuras e pinturas. Acredita-se que essas pinturas, em que os materiais mais usados são sangue, saliva, argila e excrementos de morcegos (cujo hábitat natural são as cavernas), têm cunho ritualístico.
(www.portaldarte.com.br. Adaptado.)
Todos os materiais utilizados para as pinturas, citados no
texto, são
Considere o fluxograma e as afirmações sobre as características dos referidos processos:
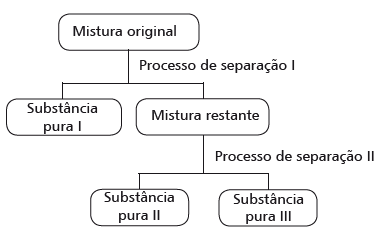
I- O processo de separação II é uma filtração. II- A mistura restante é uma solução homogênea. III- O processo de separação I corresponde a uma decantação. IV- As substâncias puras II e III correspondem a dois líquidos à temperatura ambiente.
São corretas apenas as afirmativas
Novas tecnologias de embalagens visam a aumentar o prazo de validade dos alimentos, reduzindo sua deterioração e mantendo a qualidade do produto comercializado. Essas embalagens podem ser classificadas em Embalagens de Atmosfera Modificada Tradicionais (MAP) e Embalagens de Atmosfera Modificada em Equilíbrio (EMAP). As MAP são embalagens fechadas que podem utilizar em seu interior tanto gases como He, Ne, Ar e Kr, quanto composições de CO2 e O2 em proporções adequadas. As EMAP também podem utilizar uma atmosfera modificada formada por CO2 e O2 e apresentam microperfurações na sua superfície, conforme ilustrado abaixo.

Adaptado de exclusive.multibriefs.com
O quadro fornece indicações sobre a solubilidade de alguns compostos iônicos inorgânicos em água a 20 ºC.
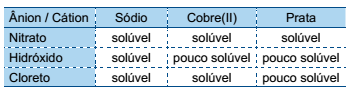
Em um laboratório, uma solução aquosa obtida a partir da
reação de uma liga metálica com ácido nítrico contém nitrato
de cobre(II) e nitrato de prata. Dessa solução, pretende-se
remover, por precipitação, íons de prata e íons de cobre(II),
separadamente. Para tanto, pode-se adicionar à mistura uma
solução aquosa de
Considere as figuras pelas quais são representados diferentes sistemas contendo determinadas substâncias químicas. Nas figuras, cada círculo representa um átomo, e círculos de tamanhos diferentes representam elementos químicos diferentes.
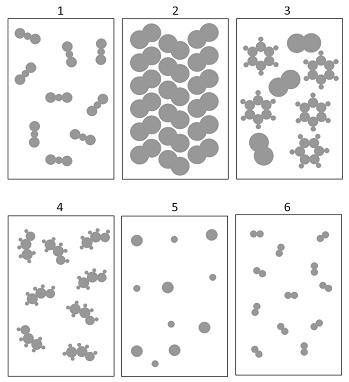
A respeito dessas representações, é correto afirmar que os
sistemas
Uma determinada quantidade de metano (CH4) é colocada para reagir com cloro (Cℓ2) em excesso, a 400 °C, gerando HCℓ(g) e os compostos organoclorados H3CCℓ , H2CCℓ2, HCCℓ3, CCℓ4, cujas propriedades são mostradas na tabela. A mistura obtida ao final das reações químicas é então resfriada a 25 °C, e o líquido, formado por uma única fase e sem HCℓ, é coletado.
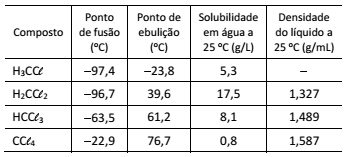
A melhor técnica de separação dos organoclorados presentes
na fase líquida e o primeiro composto a ser separado por essa
técnica são:

A pressão de vapor é uma importante propriedade físico-química das substâncias e das soluções.
Com base nos dados fornecidos e nos conhecimentos de química, é correto afirmar:
As soluções são sistemas monocomponentes e em estado líquido.
INSTRUÇÃO: Para responder à questão, analise o texto e as afirmativas que seguem.
Uma forma de gelar bebidas rapidamente consiste em preparar um recipiente com gelo e água e adicionar sal grosso ou álcool. A mistura assim produzida é denominada mistura refrigerante, pois atinge temperaturas abaixo de 0 ºC e proporciona um excelente meio de gelar as latas e garrafas colocadas dentro dele.
Sobre esse processo, afirma-se:
I. Uma mistura de gelo, água e açúcar pode ser usada como mistura refrigerante.
II. A temperatura de congelamento de uma mistura de gelo, água e areia é de cerca de 0 ºC.
III. Uma mistura de gelo, água e álcool tem duas fases e três componentes.
IV. A adição de sal grosso ao gelo com água proporciona temperaturas mais baixas do que a adição de sal fino na mesma quantidade.
De acordo com as informações acima, são corretas
apenas as afirmativas
