Questões de Vestibular
Sobre estudo da matéria: substâncias, misturas, processos de separação. em química
Foram encontradas 236 questões
1. ponto de ebulição 2. Massa 3. Volume 4. densidade
Assinale as propriedades que podem permitir ao estudante a identificação desses líquidos.
A seguir estão representadas quatro estruturas de substâncias.
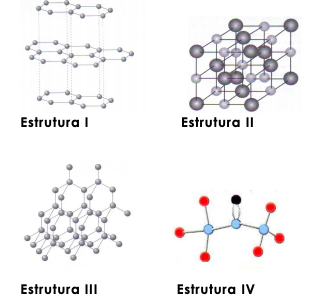
Considerando-se essas estruturas, é correto afirmar:
Acho que deveríamos consumir mais epigalocatequina-3-galato (EGCG). Isso porque a EGCG, como foi misericordiosamente abreviada, pode oferecer proteção significativa contra as duas maiores pragas de nosso tempo: o câncer e as doenças do coração. E as boas novas são que, para colher seus benefícios, não temos de engolir pílulas, beber estranhas misturas ou comer broto de feijão; só devemos adquirir o hábito de beber chá. (SCHWARCZ, J. Barbies, bambolês e bolas de bilhar. Zahar, 2009.)
Na tradicional preparação de um chá pela sua imersão em água quente é possível separar, dentre outras substâncias, o EGCG da erva utilizada.
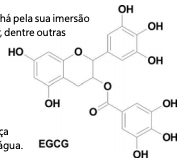
Essa separação ocorre por um método chamado:
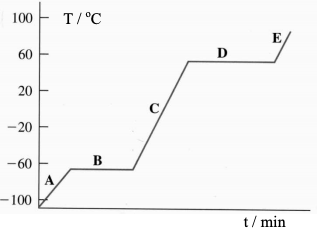
Analisando a curva, observa-se que: (a) a
temperatura de fusão; (b) a temperatura de
ebulição; (c) o estado físico do clorofórmio nos
segmentos A e D, são respectivamente:
O vazamento de petróleo, proveniente de navios petroleiros, geralmente identificado pelas grandes manchas negras de óleo sobre a superfície dos mares e sobre a areia de praias da costa brasileira, vem causando danos irreparáveis à vida marinha.
A partir dessas informações, é correto afirmar:
A: Líquida homogênea, cujos pontos de ebulição diferem em 25ºC.
B: Sólida heterogênea, composta por naftalina (naftaleno) moída e areia.
C: Sólido-líquida homogênea, composta por NaCℓ e água.
Assinale a alternativa que contém, respectivamente, os processos utilizados para a separação inequívoca dos componentes das misturas A, B e C.
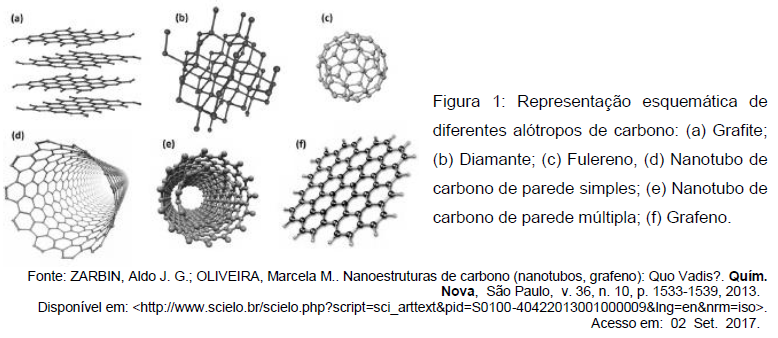
Com relação a este assunto, são feitas as seguintes afirmações.
I - O átomo de Carbono-12 possui em seu núcleo seis nêutrons e seis prótons.
II - A descoberta do C60 (Fig. 1c), que tem a forma de uma bola de futebol, impulsionou a descoberta de outras estruturas de fulerenos, principalmente materiais nanoestruturados, como os nanotubos de carbono. Estas substâncias simples possuem uma massa molar de 720 g/mol.
III - O átomo de carbono tem seis elétrons na sua eletrosfera, por isso, é chamado de hexavalente. Sendo assim, precisa apenas mais dois elétrons na sua camada de valência (camada mais externa) para obedecer à regra do octeto.
IV - Numa combustão completa, as moléculas orgânicas presentes nos combustíveis fósseis se ligam completamente ao gás oxigênio formando gás carbônico, que é um dos grandes responsáveis pelo efeito estufa.
V - Quanto à disposição dos átomos de carbono na cadeia carbônica das moléculas orgânicas, podemos classificá-las em Cadeia Normal (Reta ou Linear) ou Cadeia Ramificada.
Assinale a alternativa correta.

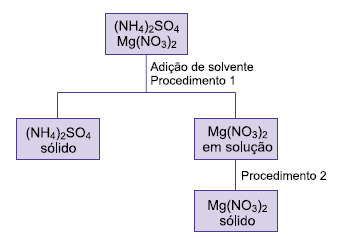
O solvente adicionado e os procedimentos 1 e 2 foram, respectivamente,


representa a curva de aquecimento, sob pressão
de 1,0 atm, em cal × °C de 10,0 g de um material
hipotético. Sobre esse material, assinale o que for
correto.

Disponível em https://www.joiabr.com.br/gem/0706.html. Acesso em: 12 out. 2015.
Sobre o texto acima, é CORRETO afirmar que:



